Introdução
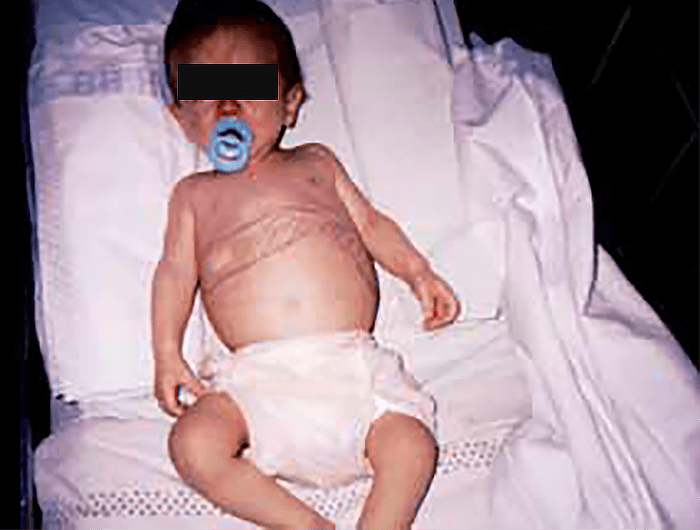
Em 1945, Spitz descreveu na criança pequena a chamada síndroma do hospitalismo e estados depressivos, relacionável com a separação da sua mãe e do ambiente da sua família em casa, e mais expressiva no contexto de hospitalizações prolongadas. Tal síndroma consiste essencialmente em manifestações de carência afectiva e em regressão no neurodesenvolvimento.
Em 1951, a Organização Mundial da Saúde publicou uma monografia da autoria de Bowlby, intitulada “Maternal Care and Mental Health”, abordando o problema da carência de cuidados maternos e sua repercussão no desenvolvimento da criança em várias situações (hospitais, creches e outras instituições).
Como conclusão de vários estudos de investigação, o referido autor lembrava aos médicos e outros profissionais de saúde uma noção fundamental: para uma boa saúde mental do lactente e criança pequena é essencial que se estabeleça um vínculo, isto é, uma relação calorosa, íntima e contínua com a mãe (ou seu substituto) conduzindo a satisfação, alegria e bem-estar a todos. Daí, o não ser desejável que em qualquer circunstância a criança se separe da mãe.
Em 1952, Robertson, em colaboração com Bowlby e Rosenbluth, demonstrando em imagens de filme os factos apontados, tentaram sensibilizar a sociedade e os profissionais para um problema que até então não era valorizado.
Posteriormente, em vários países, sobretudo da Europa e América do Norte, começou a esboçar-se uma tomada de consciência do problema, iniciando-se esforços no sentido de modificação das condições de hospitalização das crianças doentes, tornando-as mais adaptadas às suas exigências e necessidades.
Para esta tomada de consciência igualmente terá tido influência – com algum atraso – a Declaração dos Direitos Humanos em 1948, cujo artigo 25º refere o Direito da Criança a Cuidados e Assistência Especiais.
Em Portugal, três instituições foram pioneiras no cabal acolhimento e na aplicação prática de tal filosofia: Instituto de Apoio à Criança (IAC), Instituto Português de Oncologia (IPO) e Hospital Pediátrico de Coimbra (HPC). De salientar também o papel dinamizador da Sociedade Portuguesa de Pediatria, nomeadamente através da sua Secção de Pediatria Social.
Entretanto, nos EUA, nas décadas de 70-80, surgiu o conceito de Humanização, traduzindo o desenvolvimento duma estratégia ou cultura de cuidados à criança hospitalizada em ligação à mãe e família (acompanhando o doente), tornando também o ambiente hospitalar mais acolhedor com a colaboração de todos os profissionais; trata-se, pois, duma filosofia de prestação de cuidados não reduzida ao tecnicismo. Posteriormente, em 1988, viria a ser publicado um importante documento designado Carta de Direitos das Crianças Hospitalizadas.
Assim, em consonância com o conceito de Humanização, a par de medidas relacionadas com a melhoria da qualidade do atendimento nas diversas instituições, em Portugal e noutros países passou a ser cada vez mais habitual a mãe acompanhar o seu filho durante a hospitalização.
Carta de Direitos das Crianças Hospitalizadas
Este documento foi elaborado pela EACH (European Association for Child Health), aprovado em Leiden pela Confederação Europeia dos Sindicatos Nacionais e adoptado em Portugal pela Comissão Nacional de Saúde da Criança e Adolescente (CNSCA).
Descrita integralmente no capítulo 4 (Parte 1) desta obra, a referida Carta, passando a ser seguida por todos os profissionais que prestam cuidados hospitalares à criança e ao adolescente, traduz um abrir de portas das unidades de internamento ou de ambulatório às famílias segundo certas regras, as quais passaram a estar incluídas nos manuais de qualidade e segurança consagradas por legislação (DR: Lei 106/2009, 14 de Setembro).
Constando tal Carta de 10 regras, destacam-se três:
- As crianças somente serão admitidas para internamento hospitalar se os cuidados de que necessitam não puderem ser propiciados no domicílio ou em regime ambulatório.
- Os pacientes, com idade até aos 18 anos, internados em hospital ou unidade de saúde, têm direito ao acompanhamento permanente do pai e da mãe, ou de pessoa que os substitua.
- As crianças hospitalizadas devem ser agrupadas de acordo com as idades e separadas dos serviços para adultos.
No âmbito da organização e prestação dos cuidados especializados na idade pediátrica, importa uma referência especial a duas modalidades assistenciais seguindo os princípios da Humanização e da Qualidade: trata-se efectivamente de dois conceitos que permitem maior proximidade às famílias e melhor gestão de vagas de camas hospitalares: hospital de dia pediátrico e hospitalização domiciliária pediátrica, discriminados a seguir.
# Hospital de dia pediátrico – principais características (ver caixa):
|
A propósito desta modalidade, importa realçar o seguinte:
- Papel especialmente relevante no contexto de doença crónica (situação surgindo com uma prevalência de cerca de 20% da população até aos 18 anos de idade);
- Conquanto o título (hospital…) Possa gerar confusão, trata-se duma modalidade, considerada de ambulatório.
# Hospitalização domiciliária pediátrica (HDP).
Este último tópico, que na área pediátrica e no nosso País inicia os primeiros “passos”, constitui o objectivo principal deste capítulo.
Conceito de hospitalização domiciliária
Como facto histórico, importa referir que o conceito de “hospital em casa” surgiu pela primeira vez em 1947, nos Estados Unidos da América do Norte/EUA, com uma prática de cuidados médicos assistenciais em adultos designada por Home Care.
Ao tempo, com tal prática, tentava-se reduzir a taxa ocupacional dos hospitais, ao mesmo tempo que se criava um ambiente mais “humanizado”, próximo das famílias. Cerca de uma década depois, o modelo começou a ser praticado na Europa, mais propriamente, em França.
Trata-se, pois, dum modelo de prestação de cuidados em casa, dirigido a pacientes com doença aguda ou crónica, incluindo patologia complexa.
Constituindo uma alternativa ao internamento hospitalar convencional sob a responsabilidade duma equipa de saúde coordenada por médico, em ligação a serviço hospitalar clássico, para a referida hospitalização domiciliária é exigida a obediência a um conjunto de critérios clínicos, geográficos e sociais (incluindo acordo com o paciente ou familiar)
Numa perspectiva de visão holística do doente e considerando a pediatria como uma medicina integral de grupo etário, os princípios gerais enunciados deste modelo aplicam-se à idade pediátrica (< 18 anos), período da vida em que a doença crónica surge com uma prevalência relevante, atrás referida.
Objectivos da hospitalização domiciliária pediátrica (HDP)
Sistematizam-se os principais objectivos:
- Promover o bem-estar do doente e a sua recuperação, contribuindo para a melhoria da qualidade de vida de todo o agregado familiar;
- Encurtar o tempo de hospitalização e evitar internamentos frequentes, desnecessários, rendibilizando recursos;
- Estabelecer a comunicação entre os diversos níveis de cuidados, actuando em rede e promovendo a continuidade assistencial;
- Valorizar o conceito de cuidados de saúde centrados na família e a prática da educação para a saúde.
Vantagens
Como principais vantagens, citam-se:
- Favorecer o neurodesenvolvimento, diminuindo o risco de hospitalismo;
- Diminuir o risco de infecções associadas aos cuidados de saúde;
- Diminuir os custos familiares (por ex., com deslocações, alimentação, absentismo laboral, etc.;
- Promover o trabalho em equipa, com a participação da família, assessorando a equipa de saúde.
Requisitos exigidos
Eis os requisitos obrigatórios:
- A aceitação por parte da família desta modalidade de cuidados, a qual deve ser voluntária, não imposta;
- Estabilidade clínica do paciente, não se prevendo agravamento a curto prazo, exceptuando situações assistidas no regime de cuidados paliativos;
- Garantia da família quanto à assunção de responsabilidade e de disponibilidade permanente quanto a contacto telefónico ou através doutros meios de comunicação mais sofisticados;
- Ambiente doméstico com condições logísticas e sanitárias garantindo segurança.
Tipologia dos pacientes com indicação para HDP
É a seguinte:
- Doentes crónicos complexos, com falência de um ou mais órgãos (por ex. encefalopatias, cardiopatias, displasia broncopulmonar grave, síndromas polimalformativas, doenças do foro oncológico, etc.);
- Doentes submetidos a antibioticoterapia endovenosa, quer em situações crónicas, quer agudas (por ex. infecções das partes moles, osteomielites, celulites orbitárias, endocardites, empiemas, infecção por cateter, etc.);
- Doentes crónicos do foro respiratório dependentes da ventilação e/ou da oxigenoterapia, com ou sem traqueostomia;
- Doentes assistidos no regime de cuidados paliativos; sobre esta modalidade, sugere-se ao leitor a consulta de capítulos próprios nas partes I e XXXI;
- Recém-nascidos pré-termo pesando entre 1.600 gramas e 2.000 gramas, com alta hospitalar precoce;
- Necessidade de nutrição enteral ou parenteral;
- Necessidade de quimioterapia;
- Necessidade de transfusão de componentes hemáticos;
- Status pós-operatório de situações obrigando a vigilância contínua e a cuidados prolongados.
Equipa assistencial
A equipa de saúde da HDP (médica e de enfermagem), conduzida por um chefe, conta com o apoio de pessoal administrativo (fundamental para a gestão das admissões e de certa burocracia como a organização de processos e de relatórios clínicos), assim como de elementos da família e de auxiliares de acção médica. Em situações especiais, como no âmbito dos cuidados paliativos, prevê-se a colaboração de psicólogo.
No que respeita ao perfil dos elementos médicos e de enfermagem, são salientados dois tipos de pressupostos:
- Experiência clínica abrangendo o amplo grupo etário pediátrico, desde o período neonatal até ao fim da adolescência ( 0 à < 18 anos);
- Competência técnica no que respeita, designadamente, a ventilação mecânica, oxigenoterapia, nutrição enteral e parenteral, cateterismo central, canalização de veias periféricas, diálise peritoneal, transfusões, estomas, etc..
Aspectos organizativos
Seguidamente são sistematizadas de modo sucinto as principais características do funcionamento e manutenção da HDP.
Origem dos doentes: diversas dependências do hospital, desde cuidados intensivos, urgência, serviço hospitalar, hospital de dia, consulta externa, etc., até mesmo do próprio domicílio nos casos de anterior período de HDP.
Responsabilidade pela admissão em HDP: o médico hospitalar, assistente do paciente em causa, propondo à família e/ou paciente (tratando-se de adolescente) a modalidade assistencial de HDP. Nesta fase, é avaliada a eventual necessidade de dispositivos ou equipamento específico em função da patologia em causa (por ex. nebulizadores, bombas de perfusão, equipamento para oxigenoterapia em alto débito, etc.).
Área geográfica (distância entre local do hospital e local do domicílio): no caso de o doente com a indicação para HDP necessitar de transferência por qualquer razão do foro médico, importa que o tempo da transferência não seja superior a 20-30 minutos.
Formação teórico-prática dos elementos da família que autorizaram e assumiram a responsabilidade de colaboração na HDP; tal formação, na vertente teórica, poderá concretizar-se, por ex., através de material didáctico em papel, vídeo, DVD, etc. sobre problemas de saúde em geral; na vertente prática, cita-se como exemplo o tema sobre reanimação cardiorrespiratória, empregando modelos/ manequins de simulação, etc..
Garantia de meio de transporte para deslocação dos elementos da equipa ao domicílio: táxi, veículo próprio, etc..
Horário de trabalho: em condições ideais, a unidade de HDP presta assistência continuada 24 horas/dia, 365 dias/ano; contudo, por carência de recursos, tal não sendo possível, a alternativa é garantir a assistência entre 8-12 horas/dia, muitas vezes apenas nos dias úteis, gerindo o tempo e a periodicidade das visitas em função da patologia e do estado clínico. Fora do dito horário, está também prevista a modalidade não presencial de contacto telefónico diário com a família, designadamente utilizando por ex. as modalidades de sms, correio electrónico, vídeo-chamada, zoom ou skype.
Assistência integral: numa perspectiva holística, reforça-se a ideia de que é fundamental o trabalho multidisciplinar com a colaboração de todos os elementos da equipa, sendo desejável que exista contacto periódico com o médico de família responsável pelo paciente no âmbito dos cuidados primários/ centro de saúde. Aliás, numa fase de transição, está previsto que o médico de família possa integrar algumas das visitas da equipa ”titular” e, obrigatoriamente, aquando do dia em que termine o período assistencial a cargo da HDP (“alta” do paciente pela equipa de HDP).
Nota final: como foi referido no início, o funcionamento pleno da modalidade HDP, exigindo recursos, no nosso meio está ainda numa fase muito “embrionária”.
BIBLIOGRAFIA
Aujard Y. Problèmes d’actualité en néonatologie. Arch Pédiatrie 2017;24:792-794
Berry JG, Hall M, Dumas H, et al. Pediatric hospital discharges to home health and postacute facility care: a national study. JAMA Pediatr. 2016 Apr;170(4):326-33. doi: 10.1001/jamapediatrics.2015.4836.
Blackburn F, Butler M, Cheung CR. The paediatrician will hear you now’: making virtual outpatient consultations work for children and young people. Arch Dis Child Epub ahead of print: [18 Jan 2021]. doi:10.1136/archdischild-2020-321021
Boss RD, Raisanen JC, Detwiler K, et al. Lived experience of pediatric home health care among families of children with medical complexity.Clin Pediatr (Phila) 2020;59:178-187. doi: 10.1177/0009922819894006.
Bowlby J. Maternal Care and Mental Health. Geneva:WHO Monograph Series, number 2, 1951
Bowlby J, Robertson J, Rosenbluth D. A two-year old goes to hospital. Psychoanal Study Child 1952;7:82-94
Caetano E. O Internamento em Hospitais. Lisboa: Fundação Calouste Gulbenkian, 2002
Chandler AL, Beavers JC, Hall RW. Telemedicine in Pediatrics: possibilities and pitfalls. Pediatr Rev 2020;41:376-378
Collins CT, Makrides M, McPhee AJ. Early discharge with home support of gavage feeding for stable preterm infants who have not established full oral feeds. Cochrane Database Syst Rev 2015; 8:CD00374–379
Comissão Nacional de Saúde da Criança e do Adolescente (2004-2008). Lisboa: Alto Comissariado da Saúde, 2009
Cooley WC, McAllister JW, Sherrieb K, et al. Improved outcomes associated with medical home implementation in pediatric primary care. Pediatrics. 2009 Jul;124(1):358-64. doi: 10.1542/peds.2008-2600.
Crenn-Hebert C, Menguy C. Place de l’hospitalisation à domicile (HAD) dans le parcours des nouveau-nés en Île-de-France. Étude PERINAT-ARS-IDF 2017. http://www.perinat-ars-idf.org/ downloads/rapport_HAD_NN_juin2017. pdf
Elias ER, Murphy NA, et al. Home care of children and youth with complex health care needs and technology dependencies. Pediatrics 2012;129:996-1005
Fuente DO, Martinez AM, Fouces IG, Peiró S. Es necessário hospitalizar a tantos niños, durante tantos dias? La hospitalización innecesaria en pediatria. Anales Esp Pediatr 1999;50:373-378
Frush BW. Preparing residents for children with complex medical needs. Pediatrics, May 2020;145 (5):e20191731
Garcia JJ, Cruz O, Mintegi S, Moreno JM (eds). M Cruz Manual de Pediatria. Madrid: Ergon, 2020
Homer CJ, Klatka K, Romm D, et al. A review of the medical home for children with special health care needs. Pediatrics 2008;122:e922-e937
Israelsson-Skogsberg A, Persson C, Markström A, Hedén L. Children with home mechanical ventilation-Parents’ health-related quality of life, family functioning and sleep. Acta Paediatrica 2020;109:1807-1814
Kliegman RM, StGeme JW, Blum NJ, Shah SS, Tasker RC, Wilson KM (eds). Nelson Textbook of Pediatrics. Philadelphia: Elsevier, 2020
Kline MW, Blaney SM, Giardino AP, Orange JS, Penny DJ, Schutze GE, Shekerdemien LS (eds). Rudolph’s Pediatrics. New York: Mc Graw Hill Education, 2018
Levy ML, Moleiro A, Carvalho MCA, Fernandes MJ. Humanizar o Atendimento à Criança. Lisboa: Sociedade Portuguesa de Pediatria/Secção de Pediatria Social, Nestlé Portugal, 1991
Libby RC, Imaizumi SO (eds). Guidelines for Pediatric Home Health Care. Elk Grove Village, IL: American Academy of Pediatrics. Section on Home Care, 2009
Lichstein JC, Ghandour RM, Mann MY. Access to the medical home among children with and without special health care needs. Pediatrics. 2018 Dec;142(6):e20181795. doi: 10.1542/peds.2018-1795.
Maynard R, Christensen E, Cady R, et al. Home health care availability and discharge delays in children with medical complexity. Pediatrics 2019 Jan;143(1):e20181951. doi: 10.1542/peds.2018-1951.
Moro M, Málaga S, Madero L (eds). Cruz Tratado de Pediatria. Madrid: Panamericana, 2015
NHS England and NHS Improvement. Clinical guide for the management of remote consultations and remote working in secondary care during the coronavirus pandemic, 2020. In January 18, 2021: https://www.england
Ragavan MI, Marcil LE, Garg A. Climate change as a social determinant of health. Pediatrics, May 2020;145(5):e20193169
Royal College of Physicians. Future Hospital programme: delivering the future Hospital. London: RCP, 2017
Royal College of Physicians. Outpatients: The future – adding value through sustainability. London: RCP, 2018
Salisbury C, Murphy M, Duncan P. The impact of digital-first consultations on workload in general practice: modeling study. J Med Internet Res 2020;22:e18203
Sanz MTG, Oubiña LD, Barcala FJG. Home hospitalization in pulmonology: Efficient management and high patient satisfaction. Arch Broncopneumol 2020;56:479-480
Sia C, Tonniges TF, Osterhus E, Taba S. History of the medical home concept. Pediatrics 2004;113(5 Suppl):1473-1478
Simpser E, Hudak ML. Home care and child health financing. Pediatrics 2017;139(3):e20164202; DOI: https://doi.org/10.1542/peds.2016-4202
Slaper MR, Conkol K. Health tools for the pediatric patient-centered medical home. Pediatr Ann 2014;43:e39-43. doi: 10.3928/00904481-20140127-09
Spitz RA. Hospitalism. An inquiry into the genesis of psychiatric conditions. Psychanal Study Child 1945;1:53-74
Watterberg K, Committee on fetus and newborn, AAP. Providing care for infants born at home. Pediatrics, May 2020, 145 (5) e20200626