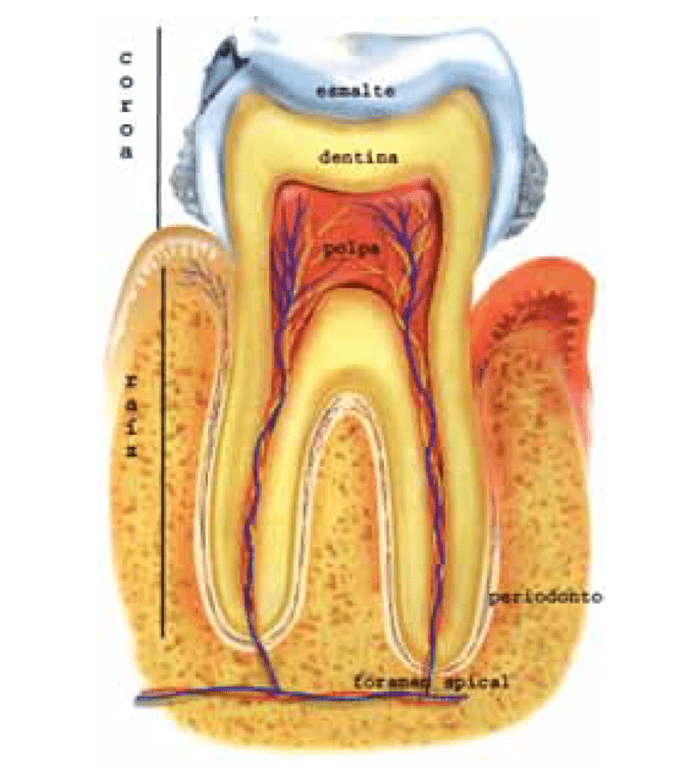
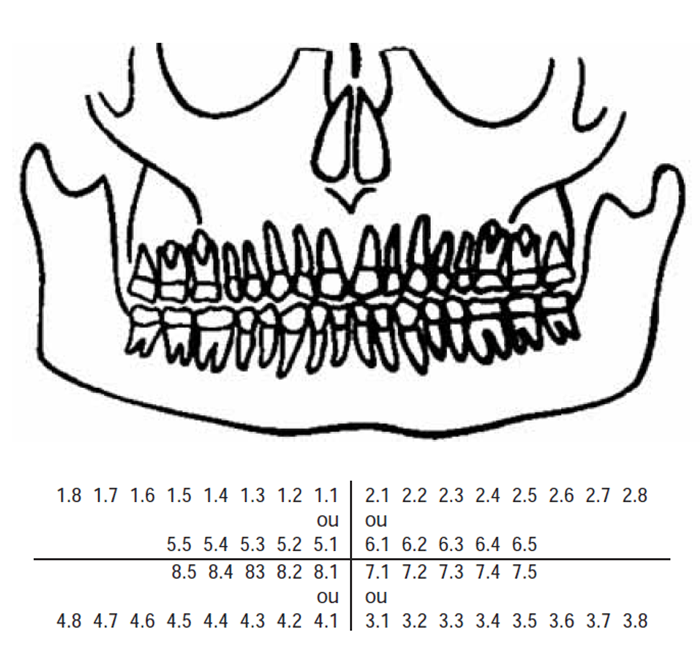
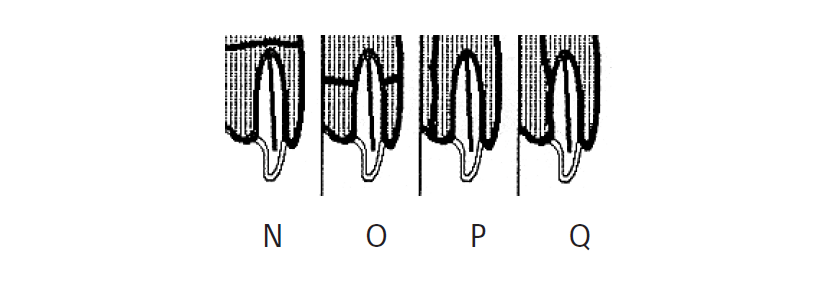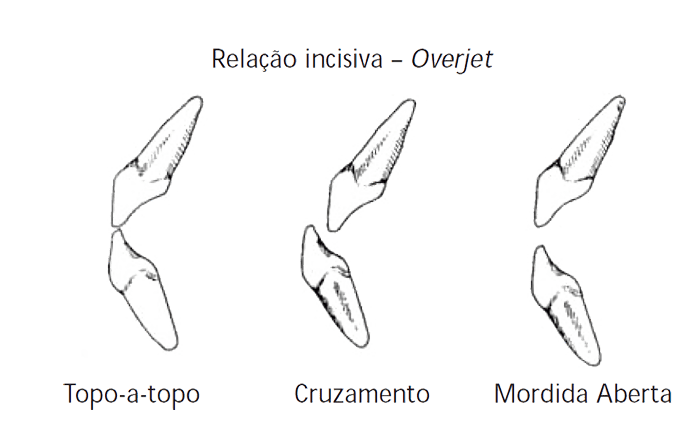Etiopatogénese e quadros clínicos
Entende-se por infecção odontogénica aquela que provém de um dente ou dos tecidos que o envolvem.
Nas alíneas seguintes são abordados os quadros clínicos mais frequentes englobados no conceito atrás expresso, estabelecendo uma relação integrada entre a etiopatogénese e sintomatologia.
Periodontite aguda e abcesso
A periodontite aguda, ou infeção aguda dos tecidos peridentários tende a estender-se a partir do apex e culminar no abcesso alveolar agudo. À sensação de (“o meu dente cresceu”) pode associar-se mobilidade relativa e dor lancinante e pulsátil.
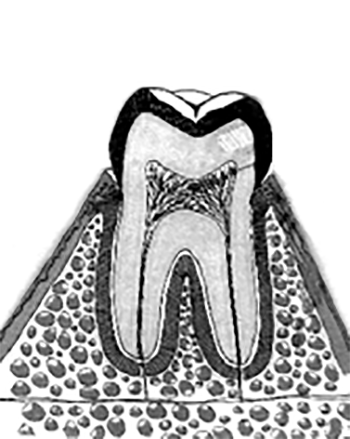
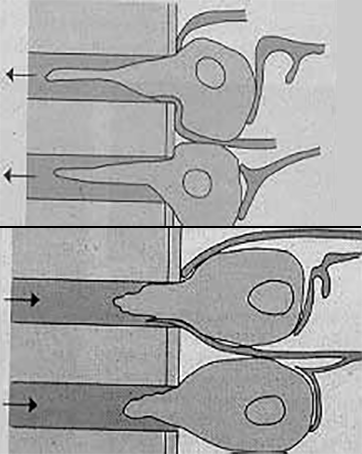
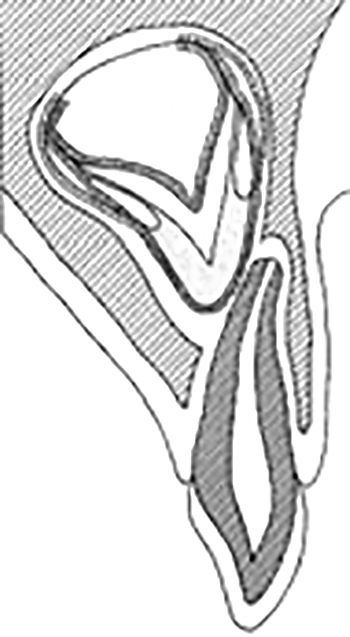
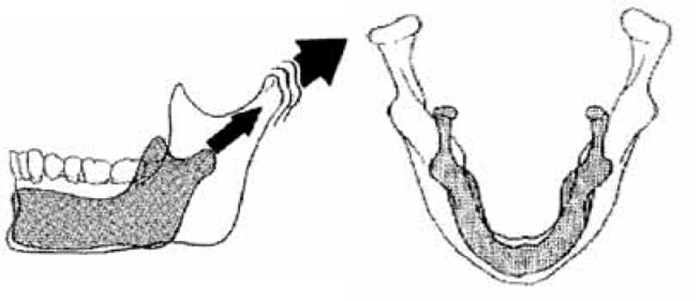
O abcesso alveolar agudo pode drenar pelo estabelecimento de fístula. A supuração pode seguir o caminho de menor resistência – o espaço ligamentar – esvaziando-se por pequeno orifício, no sulco gengival; é a fístula periodontal, mais frequente na mandíbula. (Figura 1-A)
Pode, em contrapartida, a partir do osso esponjoso, perfurar a cortical, drenando ainda para o sulco, mas poupando a zona periodontal; é a fístula gengival. (Figura 1-B)
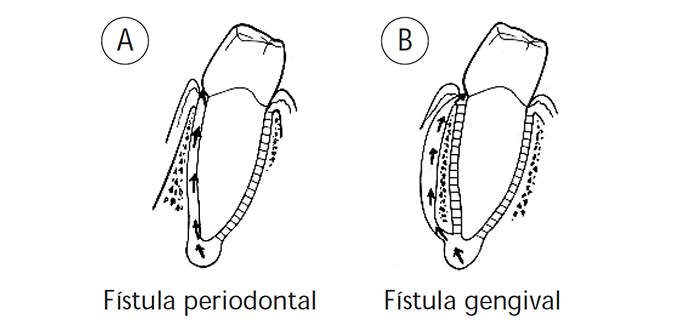
FIGURA 1. Evolução da periodontite
O abcesso alveolar agudo pode, assim, surgir na evolução natural da periodontite aguda.
Mas é mais frequente o referido abcesso enxertar-se numa inflamação ou infecção crónica, (granuloma periapical), do seguinte modo: pulpite induzindo periodontite (inflamação ligamentar) seguida de necrose do osso alveolar e colonização por microrganismos.
Salienta-se que a infecção de um dente decíduo poderá comprometer o desenvolvimento do dente definitivo sucessor.
Por outro lado, há que admitir a possibilidade (rara) de sépsis.
Granuloma e quisto periapicais
O chamado granuloma periapical corresponde a um foco de tecido de granulação circundado por uma cápsula de tecido conjuntivo fibroso; é constituído por fibroblastos e células inflamatórias, sobretudo macrófagos, linfócitos e plasmócitos. A maioria dos linfócitos é do tipo T, admitindo-se que estes tenham papel na produção do factor activador dos osteoclastos, os quais são responsáveis pela reabsorção, quer óssea, quer radicular que se lhes associa.
É a mais frequente sequela das pulpites e assinala uma competente barreira imunológica; pelo seu desenvolvimento – tantas vezes subclínico – pode constituir um mero achado radiológico, quando já possui volume bastante. Tende a apresentar, então, como sinal, uma hipertransparência periapical óbvia, redonda ou ovalada, apensa à extremidade de uma raiz, de limites bem definidos, ou mesmo limitada por linha osteosclerótica (marcadora de lento crescimento).
Apresenta semelhanças evidentes com o quisto periodontal apical; o quisto, porém, por definição, tem parede com revestimento epitelial e conteúdo líquido. Ambos assinalam a necrose pulpar.
Osteomielite
O processo séptico – quer se trate de circunstância aguda ab initio, quer se trate de agudização de lesão crónica – na maioria das vezes decorre sem grande compromisso sistémico, apesar de se lhe poder associar síndroma febril e linfadenopatia regional.
Tendo em conta que as raízes dentárias são intra-ósseas, o abcesso alveolar agudo representa já uma forma de compromisso da medular, isto é, representa uma forma localizada de osteomielite; a sua extensão significativa – em superfície e volume – pode originar osteomielite supurada.
Trata-se dum quadro de maior morbilidade que implica necessidade de vigilância rigorosa e medidas adiante discriminadas.
Celulite
As celulites odontogénicas decorrem habitualmente com alterações significativas da função fagocitária e deficiência da imunidade celular e humoral.
O quadro de celulite resulta da disseminação da infecção odontogénica estendendo-se, directa ou indirectamente, ao tecido célulo-adiposo maxilofacial e/ou cervicofacial.
O seu microbioma é, porém, sobreponível à que caracteriza outras infecções odontogénicas de menor relevo, como o abcesso alveolar agudo. É geralmente mista, predominando a associação de Streptococcus (viridans, milleri, sanguis), com Prevotella, Peptostreptococcus e fusobactérias. O seu reconhecimento através de exame cultural é fundamental.
A celulite odontogénica mais frequente, no entanto, não se desenvolve segundo o modelo que tem vindo a ser descrito, isto é, a partir da necrose pulpar, por cárie.
Efectivamente, ela deriva da infecção tecidual pericoroa dentária (pericoronarite) ao nível da mucosa do bordo alveolar, e atinge, sobretudo, os molares inferiores. Na sua evolução típica há difusão da lesão endo-óssea para a submucosa, variando as manifestações clínicas em função dos limites anatómicos das locas e espaços das fáscias, assim como da relação das raízes dos dentes, quer com as tábuas mandibulares (dentes inferiores), quer com o maxilar superior. Seguidamente são exemplificadas diversas vias de difusão.
Os incisivos, caninos e primeiros pré-molares (e molares decíduos) tenderão a exteriorizar as suas infecções para a superfície vestibular; os segundos pré-molares e os primeiros molares definitivos exteriorizarão, indiferente ou simultaneamente, para as superfícies vestibular e lingual; os segundos molares definitivos e os terceiros molares (sisos) “preferirão” a tábua interna.
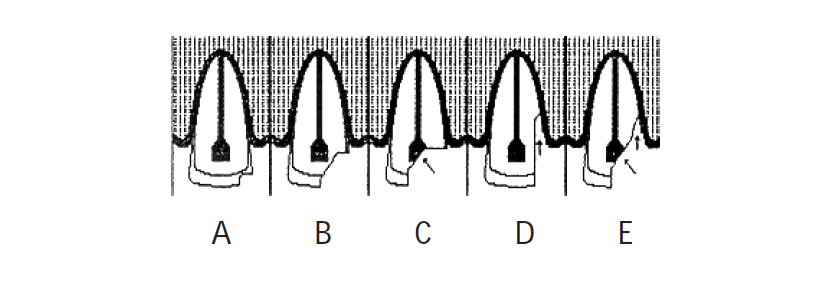
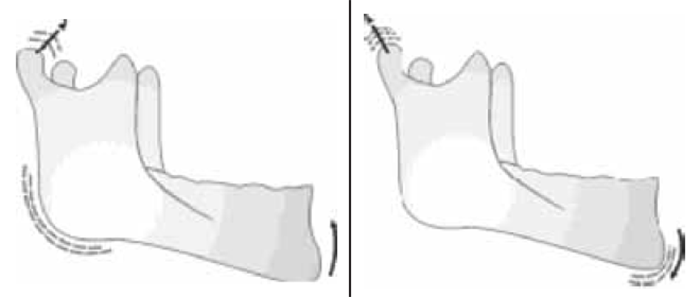
Em contrapartida, no plano vertical, a drenagem será sobretudo supra-milo-hioideia, até ao quinto dente; o sexto constitui um dente de transição, podendo o seu apex encontrar-se acima ou abaixo da inserção do músculo, mas o apex do sétimo e o do oitavo dentes são, em geral, infra-milo-hiodeus. De referir que difusão pode aparentar grandes variações. (Figura 2)
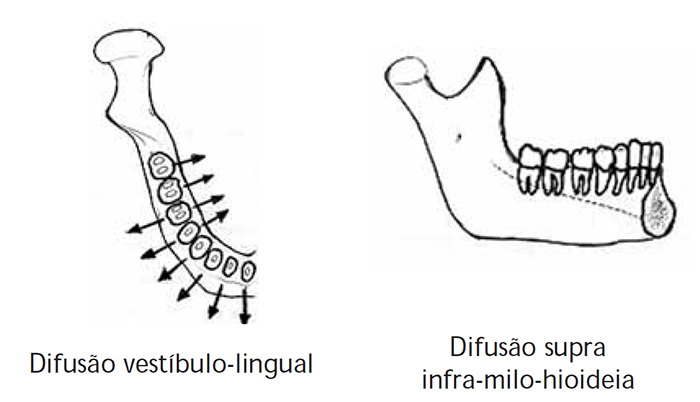
FIGURA 2. Relação das raízes dos dentes inferiores com as tábuas mandibulares: influência na evolução da celulite
Se forem consideradas as características e a topografia dos sextos dentes inferiores, aqui tomados como modelo de raciocínio, facilmente se compreende que eles podem originar, quer a tradicional celulite geniana baixa, quer uma celulite sublingual, quer uma celulite submandibular, quer ainda uma associação destas. (Figuras 3 e 3-A)
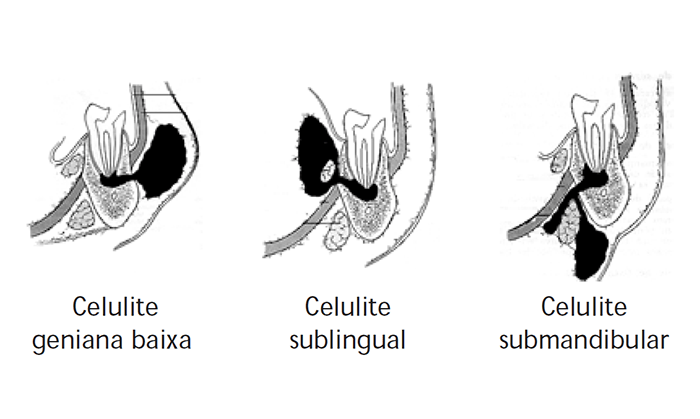
FIGURA 3. Tipos de celulite a partir de dentes do maxilar inferior
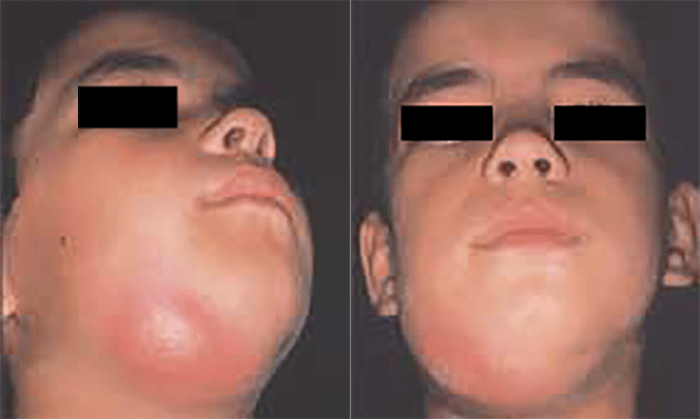
FIGURA 3-A. Celulite submandibular
Na celulite geniana baixa, a assimetria facial será óbvia pela tumefacção geniana, que pode estender-se até à região submandibular; a palpação bimanual, endo/exoral, reconhecerá a deformação do vestíbulo (espaço entre as arcadas dentárias e os lábios e bochechas), parcialmente ocupado, por oposição ao pavimento bucal e à tábua interna, incólumes.
Na celulite sublingual ou supra-milo-hioideia, a língua é empurrada para o lado oposto, pela tumefacção da área da tábua interna e poderá parecer “não caber na boca”; a glândula sublingual pode estar envolvida, e a fala e a deglutição comprometidas.
Na celulite submandibular ou infra-milo-hioideia, a palpação bimanual revela que a tumefacção se liga, quer ao bordo basilar, quer à tábua interna, se acessível, pois que o trismo pode ser a característica mais limitante. A tendência será de precoce fistulização à pele. (Figura 3)
As circunstâncias topográficas dos sextos dentes superiores – também excelentes modelos – são diferentes, mas verificam-se as mesmas condições de drenagem, com colecção aquém ou além bucinador ou, simplesmente, subperióstica (celulites geniana alta, vestibular e abcesso palatino). (Figuras 4 e 4-A)
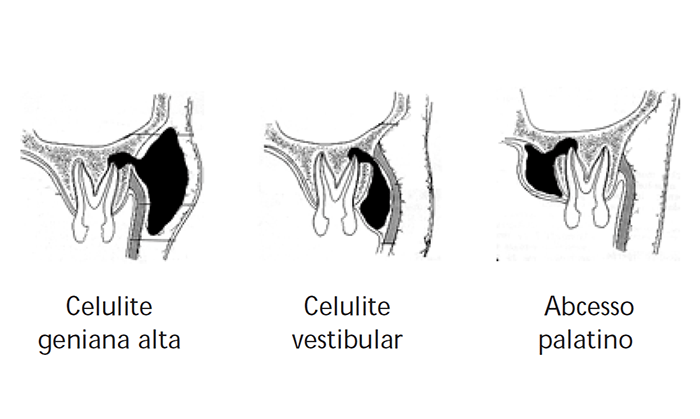
FIGURA 4. Tipos de celulite a partir de dentes do maxilar superior
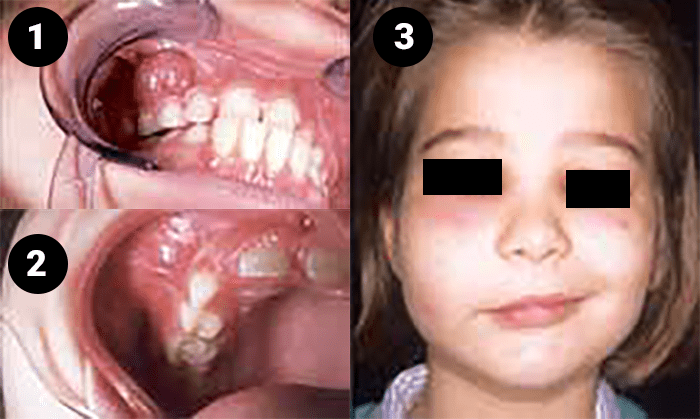
FIGURA 4-A. Infecções odontogénicas do maxilar superior
1) Abcesso vestibular; 2) Celulite vestibular; 3) Celulite geniana alta
Em qualquer das variedades anatomoclínicas, porém, o período de estado poderá implicar – para além da tumefacção e de possível linfadenopatia regional – alterações do estado geral, com febre e prostração, ou dificuldade alimentar, bem como adinamia e desidratação.
Temperatura axilar superior a 38ºC, leucocitose, proteína C reactiva elevada, trismo, dificuldade respiratória, compromisso sub-milo-hioideu, ou cervical, ou orbitário, constituem factores de alerta para a indicação de internamento. Antibioticoterapia prévia sem resposta satisfatória, ou recidiva, constituem indicações absolutas de internamento.
A importância da disseminação dos agentes infecciosos pode impor a urgência de TAC, esclarecendo a eventual difusão para o espaço dos mastigadores, espaço parafaríngeo e espaço retrofaríngeo, locas parotídea, submandibular e sublingual.
Evolução
É sobejamente conhecida a possível evolução desfavorável das infecções odontogénicas que podem disseminar-se fáscia a fáscia, espaço a espaço, acarretando risco de vida. São, exemplos, a fascite necrosante cervical, com ou sem mediastinite subsequente, a trombose do seio cavernoso, e o abcesso cerebral.
Tratamento antimicrobiano
Descreve-se, a seguir a actuação prática empírica em três situações-tipo.
Periodontite aguda e abcesso alveolar agudo
Tendo em consideração a etiologia mais provável (microflora da cavidade bucal e Streptococcus viridans) os antibióticos de primeira linha são a amoxicilina (associada ou não ao clavulanato); como alternativa poderão ser utilizados macrólidos (eritromicina, claritromicina ou azitromicina).
A duração do tratamento é 7 a 10 dias (3 a 5 dias para a azitromicina).
Salientando-se o apoio indispensável do estomatologista, poderão estar indicadas incisão e drenagem.
Celulite
Sendo implicados mais provavelmente Hemophilus influenzae do tipo B (mais raro nos vacinados anti-Hib), Staphylococcus aureus e Streptococcus pyogenes, a primeira escolha deverá ser: cefuroxima ou amoxicilina/clavulanato; como alternativa: cefalosporina de terceira geração. Se for identificado o agente, deverá utilizar-se penicilina para S. pyogenes; ou flucloxacilina para S. aureus. Como alternativas podem ser utilizados: cefalosporina de 1ª geração; ou clindamicina para os casos de S. aureus ou S. pyogenes; ou cefalosporina de 3ª geração para os casos de H. influenzae.
A duração do tratamento (eventualmente em regime de internamento hospitalar) é 7-10 dias.
Osteomielite
Em lactentes e crianças até aos 5 anos de idade os agentes patogénicos são, em geral, sobreponíveis aos da celulite.
Após os cinco anos, praticamente estão geralmente implicados os Gram-positivos. De um modo geral poderão ser utilizados os critérios referidos para a celulite.
GLOSSÁRIO
Apinhamento > Má-posição dentária provocada pela falta de espaço para acomodação dos dentes nas arcadas ósseas (desalinhados e “amontoados”).
Arcada > Conjunto formado pela estrutura da(s) dentição(ões) natural(ais) e do bordo ósseo alveolar. É o arranjo em forma de “u” dos dentes superiores e inferiores.
Avulsão > Acção de extracção ou arrancamento.
Bloco incisivo superior ou inferior > Conjunto dos incisivos centrais e incisivos laterais da arcada superior ou inferior.
Bordo incisal > Bordo cortante, existente na extremidade da coroa dos dentes anteriores.
Cúspide > Elevação piramidal da superfície oclusal ou mastigatória dos molares e pré-molares. Saliência, ponta ou convexidade.
Diâmetro mesiodistal > Distância entre a face mesial e a face distal de um dente. (ver adiante)
Diâmetro transverso de incisivo > Distância entre a face mesial e a face distal de um incisivo; corresponde à “largura” do dente.
Fossa central > Depressão arredondada de localização central nas superfícies oclusais dos molares.
Hipossialia > Défice de secreção salivar.
Mesial > O adjectivo mesial designa as áreas ou superfícies dentárias voltadas para a porção anterior dos maxilares; usa-se por oposição a distal (referente às superfícies voltadas para a porção posterior dos maxilares).
Mordida > Contacto entre os dentes superiores (maxilares) e os dentes inferiores (mandibulares); sinónimo de oclusão.
Mordida aberta > Anomalia da oclusão em que se verifica ausência de contacto vertical entre os dentes superiores e inferiores, ao morder; na mordida aberta anterior, verifica-se ausência de contacto entre os incisivos superiores e inferiores.
Mordida profunda > Anomalia da oclusão inversa à mordida aberta; quando os dentes posteriores estão em contacto, os incisivos superiores chegam a “tapar” completamente os inferiores, que podem contactar directamente a mucosa do palato.
Oclusão > Situação de contacto entre os dentes superiores e os inferiores quando os dois maxilares se aproximam.
Ortodôncia ou ortodontia > Área da Medicina Dentária dedicada à prevenção e tratamento das posições defeituosas dos dentes.
Perímetro ósseo da arcada > Medida do comprimento do rebordo ósseo alveolar, onde se inserem os dentes.
Prognatismo > Saliência dos maxilares para a frente.
Relação molar > Distância entre as faces distais do primeiro molar superior e inferior, medida sobre o plano oclusal.
Sinartrose > Articulação imóvel na qual as peças ósseas se encontram em continuidade uma com a outra.
Sincondrose > Sinartrose em que a união das peças ósseas é assegurada por tecido cartilagíneo.
Superfície palatina > O mesmo que superfície lingual; o termo usa-se exclusivamente nos dentes superiores.
Superfície vestibular > Superfície dentária que se encontra voltada para o vestíbulo.
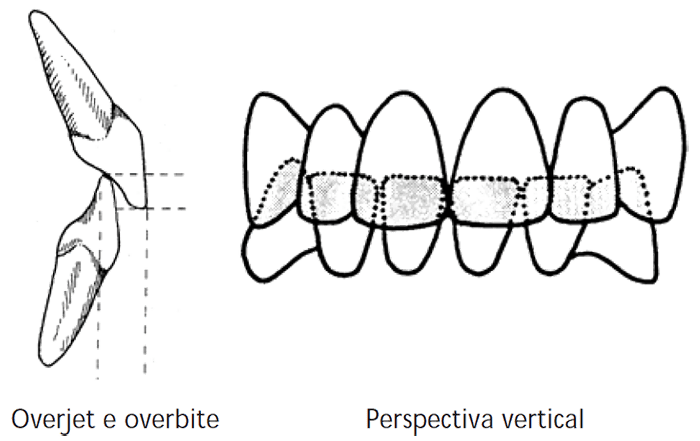
Trespasse vertical > Distância no sentido vertical entre os bordos incisais dos incisivos central superior e inferior; é internacionalmente designado por overbite.
Trespasse horizontal > Distância no sentido horizontal entre os bordos incisais dos incisivos central superior e inferior; é internacionalmente designado por overjet.
Xerostomia > Secura da boca por défice ou ausência de secreção salivar.
BIBLIOGRAFIA
American Academy of Pediatrics. Section on Breastfeeding. Breastfeeding and the use of human milk. Pediatrics 2012; 129: e827-831
American Academy of Pediatrics. Section on Pediatric Dentistry and Oral Health. Preventive oral health intervention for pediatricians. Pediatrics 2008; 122: 1387-1391
American Academy of Pediatric Dentistry. Policy on oral and maxillofacial surgery for infants, children, and adolescents. Pediatr Dent 2003; 25: 116-119
American Academy of Pediatric Dentistry. Policy on prevention of sports-related orofacial injuries. Classifications, consequences and preventive strategies. Pediatr Dent 2003; 25: 37-41
Andreasen JO, Andreasen FM, Bakland LK et al: Traumatic Dental Injuries: AManual. Copenhagen: Munksgaard, 1999
Andreasen JO, Andreasen FM: Classification, etiology and epidemiology of traumatic injuries. In Andreasen JO, Andreasen FM (eds) Textbook and Color Atlas of Traumatic Injuries to the Teeth. Copenhagen: Munksgaard, 1993, 151-177
Areias C, Macho V, Bulhosa JF, et al. Saúde oral em Pediatria Acta Pediatr Port 2008; 39: 163-170
Berkovitz Rj. Etiology of nursing caries: a microbiological perspective. J Publ Health Dent 1996; 56: 51-55
Center for Disease Control and Prevention. Recommendations for using fluoride to prevent and control dental caries in the United States. MMWR 2001; 50 (RR14): 1-42
Clarke L, Stevens C. Preventing dental caries in children: why children’s oral health is everybody’s business. Paediatr Child Health 2019; 29: 536-542
DHHS. Oral health in America: A report of the Surgeon General. Rockville: National Institute of Dental and Craniofacial Research, 2000
Enlow DH, Hans MG. Essentials of facial growth. Philadelphia: Saunders, 1996.
Erikson PR, McClintock KL, Green N. Estimation of the cariesrelated risk associated with infant formulas. Pediatr Dent 1998; 20: 395-403
Goldman L, Schafer AI (eds). Goldman-Cecil Medicine. Philadelphia: Elsevier Saunders, 2016
Green M, Palfrey JS. Bright Futures: Guidelines for Health Supervision of Infants, Children and Adolescents. Arlington: National Center dor Education in Maternal and Child Health, 2000
Griffen Al (ed). Pediatric oral health. Pediatr Clin North Am 2000; 47
Hale KJ. AAP Section on Pediatric Dentistry. Oral health risk assessment timming and establishment of the dental home. Pediatrics 2003; 111: 1113-1116
Innes NPT, Robertson MD. Recent advances in the management of childhood dental caries. Arch Dis Child 2018; 103: 311-315
Jing D, Hao J, Shen, et al. Effect of fixed orthodontic treatment on oral microbiota and salivary proteins. Experimental and Therapeutic Medicine 2019; March 18, 2019: pgs 4237-4243.https://doi.org/10.3892/etm.2019.7401
Kliegman RM, StGeme JW, Blum NJ, Shah SS, Tasker RC, Wilson KM (eds). Nelson Textbook of Pediatrics. Philadelphia: Elsevier, 2020
Kline MW, Blaney SM, Giardino AP, Orange JS, Penny DJ, Schutze GE, Shekerdemien LS (eds). Rudolph’s Pediatrics. New York: Mc Graw Hill Education, 2018
Levy, SM. An update on fluorides and fluorosis. J Canadian Dental Association 2003; 69: 286-291
Linn YTJ, Lu PW. Retrospective study of pediatric facial cellulitis of odontogenic origin. Pediatr Infect Dis J 2006; 25: 339-342
Moyer VA. US Preventive Services Task Force Statement: Prevntion of dental caries in children from birth through age 5 years. Pediatrics 2014; 133: 1102-1111
Naido S. A profile of the orofacial injuries in child physical abuse at a children’s hospital. Child Abuse Negl 2000; 24: 521-525
Neville JL et al. Oral & Maxillofacial Pathology. Philadelphia: Saunders, 2002
Nguyen PM, Kenny DJ, Barrett EJ. Socio-economic burden of permanent incisor replantation on children and parents. Dent Traumatol 2004; 20: 123-133
Pahel BT, Rowan-Legg A, Quinonez RB. A developmental approach to pediatric oral health. Pediatr Clin North Am. 2018; 65 :885-907. doi: 10.1016/j.pcl.2018.05.003
Papageorgiou SN, Xavier GM, Cobourne MT, Eliades T. Effect of orthodontic treatment on the subgingival microbiota: A systematic review and meta-analysis. Orthod Craniofac Res 2018;21:175-185. doi: 10.1111/ocr.12237
Proffit W R, Fields W. Early Stages of Development in Contemporary Orthodontics. St. Louis: Mosby, 2000.
Programa Nacional de Promoção da Saúde Oral. Acta Pediatr Port 2005; 36: 95-96
Ritter V, Catalanotto F, Lossius M. Pediatrics in the community: “Keep smiling!” ´the Florida Fluoride Project. Pediatr Rev 2010; 31: 30-31
Roda RP, Bagán JV, Bielsa JMS, Pastor EC. Antibiotic use in dental practice. A review. Med Oral Patol Oral Cir Bucal 2007;12: E186-E192
Rompante P. Mecanismos preventivos do flúor e cárie dentária. Acta Pediatr Port 2009; 40: 223-228
Scully C. Aphtous ulceration. NEJM 2006; 355: 165-172
Selwitz RH, Ismail AI, Pitts NB. Dental caries. Lancet 2007; 369: 51-58
Sonis A, Zaragoza S. Dental health for the pediatrician. Curr Opin Pediatr 2001; 13: 289-295
Ursi WJS. Crescimento e alterações nas relações mandibulares dos 6 aos 18 anos de idade. Ortodontia 1996; 29: 4-11
WHO. Guidelines for drinking-water quality conference (Berlin, 2007). Geneva: WHO, 2007