GASTROSQUISE
Definição e importância do problema
A gastrosquise é uma anomalia congénita da parede anterior do abdómen caracterizada por:
- Ausência do encerramento da parede abdominal atingindo todas as camadas (fáscia-músculo-pele), na maioria das vezes à direita da inserção (normal) do cordão umbilical; e
- Exteriorização, por esse defeito, da parede (que varia entre 0,5 e 3 cm), de conteúdo intrabdominal.
O conteúdo intrabdominal é constituído por vísceras ocas como estômago ou ansas intestinais, não cobertas por peritoneu ou membrana amniótica (ao contrário da onfalocele).
A incidência deste defeito é cerca de 1/5.000 a 1/10.000 nascimentos não se verificando predomínio de sexos. Actualmente, de acordo com estudos de várias séries internacionais, existe uma tendência de aumento progressivo da frequência desta anomalia; as razões deste facto são desconhecidas.
Etiopatogénese e anomalias associadas
A gastrosquise (surgindo, como regra, isoladamente, ao contrário da onfalocele) é de etiologia desconhecida. De acordo com alguns estudos epidemiológicos, especula-se sobre a acção teratogénica de certas substâncias, designadamente da cocaína.
Igualmente se tem demonstrado o efeito nocivo do líquido amniótico em contacto directo com as ansas intestinais, o que é relacionado com a acção de citocinas e mediadores pró-inflamatórios como a IL-6 e IL-8. Tal efeito, intensificado proporcionalmente à duração da gestação, e mais agressivo se o líquido amniótico contiver mecónio eliminado in utero, tem sido demonstrado ao nível do plexo nervoso mientérico e das células de Cajal.
A alteração da integridade da parede abdominal poderá ser decorrente de uma regressão prematura de uma das duas artérias onfalomesentéricas. Esta regressão vascular poderá ser responsável por alterações isquémicas da parede abdominal contribuindo para o defeito morfológico fáscio-músculo-cutâneo. Alguns investigadores não distinguem a patogénese da gastrosquise da da onfalocele. Assim, a gastrosquise poderia ser originada pela ruptura do saco peritoneal que recobre as ansas intestinais.
Após o nascimento verifica-se que as ansas intestinais, pelo contacto prolongado com o líquido amniótico, estão aderentes entre si, com consistência superior ao habitual, o que é explicável pela existência de exsudado gelatinoso que as recobre como pequena “carapaça” ou peel. Este fenómeno pode originar inflamação no peritoneu (peritonite meconial), edema da parede intestinal, formação duma película de fibrose assim como compressão das artérias mesentéricas e das fibras nervosas entéricas, sendo que o próprio orifício para-umbilical poderá também ter efeito compressivo sobre os vasos; como consequências, poderão surgir:
- Ulterior desenvolvimento de volvo, estenose, atrésia e encurtamento intestinais por necrose isquémica extensa;
- Dismotilidade intestinal;
- Dificuldade na reintrodução das ansas na cavidade abdominal.
Torna-se, assim, fácil compreender as anomalias anatómicas e funcionais, sobretudo do foro digestivo que poderão acompanhar a gastrosquise, numa proporção ~10%. A má-rotação intestinal está, por definição, sempre presente na gastrosquise.
Manifestações clínicas e diagnóstico
O diagnóstico pré-natal da gastrosquise pode ser obtido nos exames ecográficos realizados após a 12-14ª semana de gestação. A imagem de exteriorização amniótica de ansas intestinais por meio de um defeito para-umbilical, não contidas num saco peritoneal é muito sugestiva; de referir que a probabilidade de diagnóstico ecográfico pré-natal de defeitos da parede abdominal, designadamente no que se refere à gastrosquise, oscila entre 57 e 95%. Em função do contexto clínico, poderá estar indicado estudo citogenético pré-natal no líquido amniótico e/ou no sangue do cordão. (Figura 1)
O soro materno em situações de gastrosquise no período pré-natal evidencia em 100% dos casos valores séricos elevados de alfa-fetoproteína. A acetil colinesterase no líquido amniótico tem também valores elevados, ao contrário do que acontece na onfalocele.
A evidência ecográfica pré-natal de gastrosquise implica necessariamente a detecção doutras anomalias acompanhantes, nomeadamente cardíacas, embora estas sejam raras, ao contrário da onfalocele.
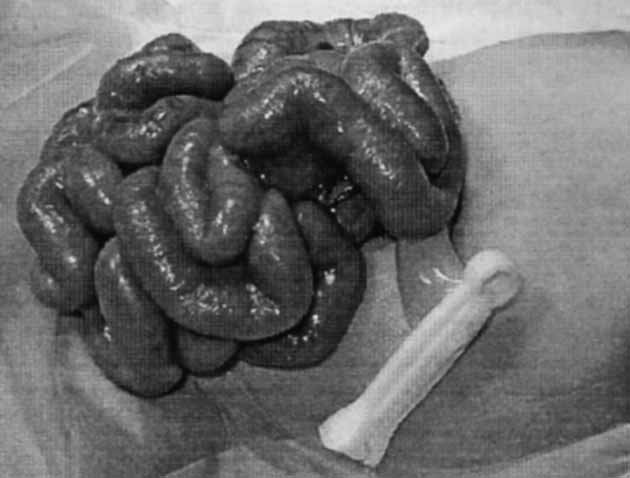
FIGURA 1. Gastrosquise (vísceras exteriorizadas sem saco) (Arq. JMVA, 1976).
O estudo ecográfico deverá incidir especialmente sobre a caracterização das ansas intestinais no que respeita ao espessamento da parede e permeabilidade do lume, aspectos que têm valor prognóstico quanto à evolução a curto, médio e longo prazo. Deverá igualmente ser realizado por amniocentese o estudo citogenético, designadamente para detecção de cromossomopatias associadas e/ou identificação de loci patológicos específicos.
Não está provado que o parto programado por via alta tenha vantagens relativamente ao parto vaginal.
No RN o diagnóstico é óbvio; contudo, deve inspeccionar-se cuidadosamente o orifício umbilical, dada a eventualidade de diagnóstico diferencial com onfalocele rota in utero (e no pressuposto de não se ter realizado ecografia pré-natal).
Sob o ponto de vista da prática clínica, a gastrosquise é habitualmente classificada utilizando uma escala de gravidade e de estratificação de risco (escala de Le Fort pontuando situações de I a IV). Com efeito, esta escala não se relaciona tanto com o diâmetro do orifício, mas com o estado de vitalidade e função global das ansas intestinais no que respeita a serosite, edema da parede, presença de atrésia e encurtamento intestinal por necrose extensa de ansa. Estes aspectos patológicos estão associados à exposição amniótica e urinária e às lesões isquémicas do intestino que podem ser originadas pela compressão vascular – mesentérica do orifício para-umbilical. (ver atrás)
A detecção de anomalias associadas deverá ser ponderada em função do contexto clínico.
Tratamento
Quanto à gastrosquise aplicam-se os mesmos princípios gerais, designadamente quanto a local do parto e cuidados pré-operatórios. Dados os efeitos lesivos do líquido amniótico e do mecónio eliminado in utero, em contacto permanente com as ansas fetais, efeitos que aumentarão com a idade gestacional, discute-se hoje sobre a decisão de antecipar o parto (segundo alguns para as 36-37 semanas) tendo em vista minorar os referidos efeitos atrás descritos.
No pós-parto imediato, a criança deve ser (também) colocada em decúbito lateral para evitar a angulação dos vasos do mesentério.
Na UCIN do Hospital de Dona Estefânia, o procedimento é o seguinte: as vísceras exteriorizadas são envolvidas com compressas esterilizadas molhadas em soro fisiológico aquecido, envolvendo-se depois aquelas num saco de plástico esterilizado ou em celofane esterilizado. Não se aplica qualquer desinfectante tópico.
O objectivo do tratamento cirúrgico da gastrosquise é a reintrodução das ansas intestinais e o encerramento primário da parede abdominal utilizando diversas técnicas que ultrapassam o âmbito deste livro.
Nos casos em que não é possível realizar o encerramento primário, pela presença de gastrosquise muito volumosa ou pelo endurecimento seroso das ansas intestinais, deverá ser proposta a contenção das ansas intestinais por meio de um saco de polímero de silastic, suturado à orla do orifício para-umbilical. Este método promove a restituição das ansas para a cavidade peritoneal por fases, com encerramento definitivo diferido.
O encerramento forçado da parede não deverá ser tentado pelos riscos apontados a propósito da onfalocele. Como particularidade relativamente à gastrosquise, cabe salientar que o encerramento sob extrema tensão, com ansas intestinais de parede edemaciada e pouco dúctil, poderá originar deiscência da sutura abdominal ou compromisso isquémico da ansa intestinal subjacente por compressão mesentérica.
Complicações pós-operatórias
As complicações pós-operatórias são decorrentes de aumento de pressão intrabdominal associadas ao encerramento primário forçado (já descritas anteriormente), ou decorrentes de complicações sépticas locais associadas à utilização de materiais heterólogos para o encerramento primário, ou secundário por fases.
É frequente verificar-se no período pós-operatório, face às alterações mecânicas, bioquímicas e neuroentéricas das ansas intestinais, um período de adaptação intestinal longo e difícil aos nutrientes por via entérica. A dependência da nutrição parentérica poderá ser prolongada, nomeadamente nos casos em que coexiste atrésia segmentar ou necrose isquémica extensa, conducente a encurtamento intestinal, com desenvolvimento de síndroma de intestino curto.
Devido à serosite parietal, poderão ocorrer com alguma frequência, quadros suboclusivos por aderências ou bridas. Estas manifestações, quando não têm resolução clínica conservadora, podem implicar terapêutica cirúrgica para excisão de bridas e aderências.
Prognóstico
O prognóstico depende fundamentalmente da existência de lesões e dismotilidade intestinais relacionadas com a eliminação de mecónio in utero, e de complicações graves de tipo mecânico, metabólico e neuroentérico. Nesta perspectiva realçam-se a síndroma de intestino curto e as complicações associadas ao cateterismo central de longa duração. A sobrevivência é actualmente cerca de 95%.
A presença de defeitos gastrintestinais associados, a prematuridade e a necessidade de introdução mais tardia da alimentação entérica por disfunção intestinal constituem factores de risco e de agravamento do prognóstico.
OUTROS DEFEITOS DA PAREDE ABDOMINAL
Aplasia da musculatura abdominal (Síndroma de Eagle Barrett)
Faz-se uma referência breve a esta síndroma rara (com uma incidência de cerca de 1/40.000 recém-nascidos), também chamada síndroma “prune belly” (aspecto de “barriga” em passa de ameixa ou de abrunho).
Trata-se da associação de aplasia da musculatura abdominal (determinando que o abdómen seja flácido e alargado para os lados, e a respectiva pele fique “engelhada”, com pregas ou ondulada), distopia testicular, e anomalias do tracto urinário relacionáveis com obstrução da uretra no período fetal: megabexiga, mega uréter, hidronefrose e graus diversos de displasia renal. Oligoâmnio e hipoplasia pulmonar constituem complicações frequentes no período perinatal. As costelas inferiores podem fazer saliência para fora, comprometendo a dinâmica respiratória, o que predispõe a infecções. As anomalias do úraco podem também fazer parte desta síndroma.
Em cerca de 10% dos casos verifica-se associação, também, a defeitos cardíacos e em 50% a anomalias do sistema músculo-esquelético. Na maioria dos casos (mais de 95%) os doentes são do sexo masculino.
Uma vez diagnosticada obstrução do uréter ou uretra, estão indicados procedimentos de drenagem emergente (vesicostomia ou pielostomia) para preservação da função renal, os quais são mantidos até à idade da intervenção cirúrgica reconstrutiva. O prognóstico depende do grau de hipoplasia pulmonar e de displasia renal. Em casos seleccionados poderá estar indicada transplantação renal.
Ectopia cardíaca (Ectopia cordis)
Esta anomalia rara traduz-se por “tumor” pulsátil situado entre o apêndice xifoideu, que é curto, e o umbigo. No sentido anatomofisiológico, a saliência pulsátil é uma hérnia cujo saco é formado pelo pericárdio. Poderá haver associação a defeitos cardíacos septais.
Úraco patente
A esta situação clínica foi feita referência no capítulo sobre Alterações da Bexiga. Recorda-se, a propósito, que úraco é a parte superior da alantoideia que se dirige para o umbigo; no embrião humano transforma-se precocemente num cordão fibroso que se estende como ligamento da bexiga ao umbigo. Excepcionalmente, essa estrutura inicialmente canalicular não se transforma em estrutura fibrosa, permitindo que, através do umbigo, seja eliminada urina; é o úraco patente. Por vezes formam-se dilatações quísticas no seu trajecto; são os quistos do úraco.
O úraco patente pode estar associado a divertículos da bexiga.
|
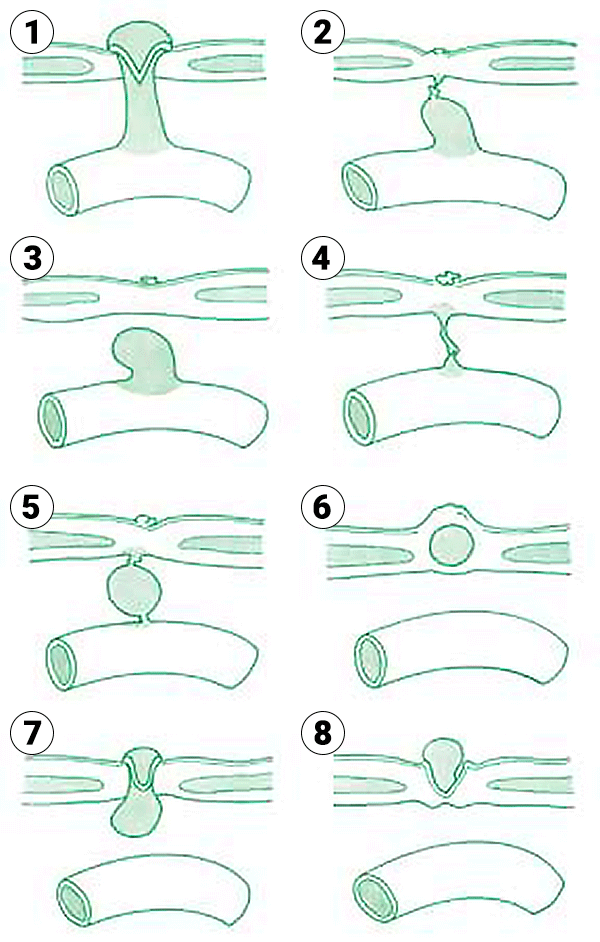
FIGURA 2. Defeitos relacionados com remanescências do canal onfalomesentérico.
Canal onfalomesentérico (ou vitelino) vestigial
Os vestígios do canal onfalomesentérico (estrutura que liga, entre a 5ª e 7ª semana de vida intra-uterina, o saco vitelino ao intestino primitivo, podem ter expressão clínica diversa ao nível da parede abdominal (Figura 2): canal patente simile fístula ligando o umbigo ao intestino delgado; corda fibrosa ligando a face interna da região umbilical ao intestino, provocando depressão ou fosseta ao nível do umbigo por retracção deste; pequeno pólipo no umbigo (cuja superfície é constituída por mucosa intestinal) associado a corda fibrosa anteriormente descrita; pequeno quisto forrado internamente por mucosa intestinal no trajecto do cordão fibroso antes referido; divertículo intestinal cujo lume comunica com intestino delgado ao nível do bordo antimesentérico, a distância variável da válvula ileocecal (divertículo de Meckel).
BIBLIOGRAFIA
Allin BSR, Hall N, Ross A, et al. Development of a gastroschisis core outcome set. Arch Dis Child Fetal & Neonatal Ed 2019; 104: F76-F82
Ashcraft KW, Holcomb GW III, Murphy JP (eds). Pediatric Surgery. Philadelphia: Saunders, 2005
Cloherty JP, Eichenwald EC, Strak AR. Manual of Neonatal Care. Philadelphia; Lippincott Williams & Wilkins, 2008
Christison – Lagay ER, Kelleher CM, Langer JC. Neonatal abdominal wall defects. Seminars in Fetal & Neonatal Medicine 2011; 16: 164-172
Coran AG. Pediatric Surgery. Philadelphia: Elsevier, 2013
Correia-Pinto J, Tavares ML, Baptista MJ, et al. Meconium dependence of bowel damage in gastroschisis. J Pediatr Surg 2002; 37: 31-35
Drongoswky R, Smith R, Coran A. Contribution of demographic and enviromental factors to the etiology of gastrosquisis: a hypothesis. F Diag Ther 1991; 6:14-17
Kliegman RM, StGeme JW, Blum NJ, Shah SS, Tasker RC, Wilson KM (eds). Nelson Textbook of Pediatrics. Philadelphia: Elsevier, 2020
Kline MW, Blaney SM, Giardino AP, Orange JS, Penny DJ, Schutze GE, Shekerdemien LS (eds). Rudolph’s Pediatrics. New York: Mc Graw Hill Education, 2018
MacDonald MG, Seshia MMK (eds). Avery’s Neonatology: Pathophysiology and Management of the Newborn. Philadelphia, PA: Lippincott Williams & Wilkins, 2015
Minkes R, Langer J, Massiotti M. Routine insertion of silastic silo for infants with gastrosquisis. J Pediatr Surg 2000; 35: 843-847
Oldham KT, Colombani PM, Foglia RP (eds). Principles and Practice of Pediatric Surgery. Philadelphia: Lippincott Williams & Wilkins, 2005
Reynolds M. Abdominal wall defects in infants with very low birth weight. Semin Pediatr Surg 2000; 2: 88-90
Snyder C. Outcome analisys for gastroschisis. J Pediatr Surg 1999; 34: 1253-1257
Walker K, Holland A. Physical growth, neurodevelopment, and cognition outcomes in children with abdominal wall defects: a tale with two endings? Arch Dis Child Fetal & Neonatal Ed 2019; 104: F2-F3
Werler MM, Sheehan JE, Mitchell AA. Association of vasoconstrictive exposures with risks of gastroschisis and small intestine atresia. Epidemiology 2003; 14: 349-354