Definição e etiopatogénese
A doença celíaca é definida como uma doença autoimune desencadeada pela exposição ao glúten (mais propriamente à sua fracção gliadina) em indivíduos geneticamente susceptíveis (possuidores de antigénios de histocompatibilidade: HLA de classe II DQ2 e DQ8).
O órgão alvo desta doença é o intestino proximal, constituindo-se uma lesão da respectiva mucosa caracterizada por um infiltrado linfoplasmocitário na lâmina própria, infiltrado linfocitário intraepitelial, hiperplasia das criptas e atrofia das vilosidades.
Aspectos epidemiológicos
Rastreios sistemáticos em populações europeias avaliando a presença de marcadores serológicos de doença celíaca demonstraram uma maior prevalência desta (1/140 a 1/300) em relação a anteriores estudos, baseados unicamente em formas sintomáticas (1/1.000 a 1/2.500). Estudos nacionais apontam, para uma prevalência de 1/134.
Assim, considera-se hoje que a “condição celíaca” constitui como que um iceberg, do qual a doença celíaca sintomática constitui a ponta visível.
Manifestações clínicas
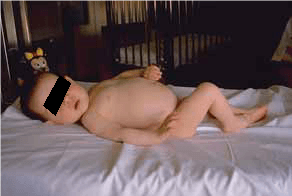
FIGURA 1. Lactente com doença celíaca. Distensão abdominal relacionável com meteorismo. (NIHDE)
A forma clássica de apresentação desta doença traduz-se por uma síndroma de má-absorção alguns meses após a introdução do glúten no regime alimentar (presente nas farinhas de trigo, centeio ou cevada), com diarreia crónica e/ou vómitos, inflexão nas curvas ponderais e estaturais (primeiro naquelas, depois nestas), distensão abdominal, atrofia das massas musculares e tecido celular subcutâneo, anorexia e alteração do humor (irritabilidade, apatia) (Figura 1).
Ao casos mais graves podem evidenciar hipoalbuminémia com edema, hipocaliémia e défice de vitamina K determinando aumento do tempo de protrombina.
No entanto, e sobretudo nas crianças mais velhas, as manifestações podem ser mais atípicas (paucissintomáticas) ou mesmo predominantemente extraintestinais (Quadro 1). A anemia por deficiência de ferro é uma forma muito frequente de manifestação extraintestinal.
Num estudo realizado em 161 crianças com a doença e seguidas com regularidade nos últimos três anos na Unidade de Gastrenterologia do Hospital Dona Estefânia, 3,7% apresentavam quadros clínicos predominantemente extraintestinais.
QUADRO 1 – Manifestações extraintestinais da doença celíaca
| Dermatológicas • Dermatite herpetiforme, alopécia, vitíligo |
| Hematológicas • Anemia isolada (ferropénica ou macrocítica por défice de ácido fólico) • Anemia hemolítica autoimune, trombocitopenia autoimune • Trombocitose (hipoesplenismo) |
| Endocrinológicas • Diabetes mellitus tipo I, tiroidite autoimune • Atraso estatural isolado, atraso pubertário isolado |
| Neurológicas • Epilepsia (com calcificações occipitais), ataxia |
| Hepáticas • Hipertransaminasemia, hepatite autoimune |
| Orais • Aftas recorrentes • Hipoplasia do esmalte dentário (dentes definitivos) |
| Osteo-articulares • Osteoporose, artralgia/artrite |
| Ginecológicas • Infertilidade, abortos de repetição |
| Psiquiátricas • Ansiedade/depressão |
De acordo com a proposta da ESPGHAN de 2012 dever-se-ão privilegiar os termos intestinais e extra intestinais para caracaterização dos sintomas ao invés de classificar a doença como típica ou atípica. Da mesma forma se poderão utilizar os termos:
- doença celíaca silenciosa ou subclínica (associada a resultados positivos de estudos serológicos, de HLA e histológicos, e a ausência de sinais clínicos);
- doença celíaca potencial(associada a presença de anticorpos – habitualmente detectados no decorrer de rastreios a grupos de risco /ver adiante – e a ausência de alterações histológicas); e
- doença celíaca latente (em indivíduos evidenciando em certa fase da doença:
- critérios de diagnóstico de doença celíaca, e ulteriormente assintomáticos e com histologia normal no contexto de dieta com glúten, ou inversamente,
- histologia normal com dieta sem restrição e ulteriormente evidenciando os característicos achados histológicos da doença.
Em suma, abaixo do “limite da visibilidade” encontram-se as chamadas formas de doença celíaca silenciosa e doença celíaca potencial e latente (como no caso de familiares de 1º grau de doentes celíacos, ou em grupos de risco, obrigando a rastreio serológico – Quadro 2). Actuamente existe a tendência geral para abandonar o termo latente.
QUADRO 2 – Grupos de risco de doença celíaca (obrigando a rastreio serológico)
| · Familiares de 1º grau · Dermatite herpetiforme · Diabetes tipo I · Tiroidite autoimune · Síndroma de Sjögren · Hemossiderose pulmonar · Síndroma de Down · Nefropatia IgA · Artrite reumatóide |
Diagnóstico
O índice de suspeita relativamente a doença celíaca deve ser bastante apurado, principalmente para as formas paucissintomáticas ou extraintestinais, bem como para os grupos de risco.
O rastreio inicial faz-se através da determinação sanguínea dos marcadores serológicos-anticorpos anti-transglutaminase tecidual de classe IgA (tTG), bem como da determinação de IgA total. (Actualmente nalguns centros europeus procede-se ao rastreio de tTG utilizando a saliva).
De acordo com a ESPGHAN, títulos no sangue de anticorpos tTG > 10 vezes o limite superior do normal, associam-se a alta probabilidade de atrofia das vilosidades intestinais.
De salientar que valor elevado de anticorpos anti-transglutaminase tecidual, nos casos de diabetes tipo 1 recentemente diagnosticada, nem sempre indica doença celíaca.
A prevalência de défice em IgA é cerca de 2-3% entre os celíacos. Esta circunstância podendo, pois, condicionar um resultado de tTG falso negativo, obrigará à análise dos anticorpos anti-transglutaminase da classe IgG. Se o resultado destes for negativo poderá considerar-se válida a serologia negativa.
Outras causas de serologia negativa de tTG são: dietas pobres em glúten, enteropatias com perda de proteínas, imunossupressão e casos de doentes com menos de dois anos.
Actualmente o uso de anticorpos antigliadina para rastreio de doença celíaco não está recomendado.
O anticorpo anti-endomísio (AAE), do tipo IgA, não faz parte do estudo inicial. As suas sensibilidade e especificidade variam com a idade. As desvantagens são o elevado custo monetário e o facto de não ser quantificável, estando a aferição da sua positividade dependente do observador.
Níveis 10 vezes superiores ao valor limite da normalidade podem ser considerados altamente específicos da doença celíaca, inclusivamente nos casos de tTG negativos.
O diagnóstico definitivo deve ser feito pela biópsia duodenal por endoscopia alta; no entanto, de acordo com as normas de orientação da ESPGHAN de 2012 a biópsia duodenal poderá ser obviada em doentes sintomáticos:
- com títulos de anticorpos tTG > 10 vezes o limite superior do normal; ou
- com anticorpos AAE positivos; ou
- com determinação positiva de tipagem HLA compatível com a doença.
Tal decisão deve ser individualizada e tomada por gastrenterologista pediátrico.
Após o diagnóstico e a instituição de dieta sem glúten, o desaparecimento de sintomas, assim como a normalização de marcadores serológicos permite confirmar o diagnóstico e avaliar a boa resposta e cumprimento da dieta.
Na ausência de resposta à dieta sem glúten, após certificação da adesão dietética, poderá ser considerada a repetição das análises e de nova bióspia.
A prova de sobrecarga com glúten, com indicações escassas e apenas em crianças com mais de 5 anos de idade, deve ser admitida se houver dúvidas quanto ao diagnóstico. A mesma deve ser precedida de nova investigação serológica e de novo estudo da tipagem HLA. A elevação dos títulos dos marcadores serológicos ou o reaparecimento de alterações histológicas após a sobrecarga reforçam o diagnóstico.
Tratamento
O tratamento baseia-se na evicção completa do glúten da dieta para toda a vida (consultar Anexos-volume 3).
Os riscos de abandono da dieta, o que sucede muitas vezes na adolescência, prendem-se com a possibilidade de aparecimento na idade adulta de doenças neoplásicas (adenocarcinoma do delgado, linfoma não Hodgkin do tubo digestivo), ou outras de grande morbilidade (osteoporose, infertilidade ou abortos de repetição, doença neurológica ou psiquiátrica).
Nas formas clássicas com desnutrição grave na data do diagnóstico poderá ser necessário recorrer a técnicas de suporte nutricional:
- alimentação entérica contínua, ou alimentação fraccionada, empregando sempre fórmulas sem lactose ou semi-elementares numa fase incial;
- suprimento de minerais (principalmente ferro e ácido fólico) e de vitaminas deficitários.
Em estudo encontram-se novas terapêuticas com enzimas (de origem bacteriana) que hidrolisam péptidos tóxicos da gliadina, ou vacinas peptídicas indutoras de tolerância.
BIBLIOGRAFIA
Antunes H. First prevalence of celiac disease in a Portuguese population. JPGN 2002; 2: 240-24 3
Antunes H, Abreu I, Nogueiras A, et al. Primeira determinação de prevalência de doença celíaca numa população portuguesa. Acta Med Port 2006; 19: 115-120
Bonamico M, Nenna R, Montuori M, et al. First salivar screening of celiac disease by detection of anti- transglutaminase autoantibody radioimmunoassay in 5000 Italian primary school children. JPGN 2011; 52: 17-20
Hill ID, Dirks MH, Liptak GS, et al. Guideline for the diagnosis and treatment of celiac disease in children: recommendations of the North American Society for Pediatric Gastroenterology, Hepatology and Nutrition/NASPGHAN. J Pediatr Gastroenterol Nutr 2005:40;1–19
Husby S, Koletzko S, Korponay-Szabó IR, et al. ESPGHAN Working Group on Coeliac Disease. Guidelines for the diagnosis of coeliac disease. JPGN 2012; 54:136–160
Kaukinen K, Lindfors K. Novel treatments for celiac disease: glutenases and beyond. Dig Dis 2015; 33: 277-281
Kliegman RM, StGeme JW, Blum NJ, Shah SS, Tasker RC, Wilson KM (eds). Nelson Textbook of Pediatrics. Philadelphia: Elsevier, 2020
Koletzko B. Pediatric Nutrition in Practice. Basel: Karger, 2008
Lindfors K, Koskinen O, Kaukinen K. An update on the diagnosis of celiac disease. Int Rev Immunol 2011; 30: 185-196
Llanos-Chea A, Fasano A. Gluten and functional abdominal pain disorders in children. Nutrients 2018;10 (10). pii: E1491. doi: 10.3390/nu10101491.
Moro M, Málaga S, Madero L (eds). Cruz Tratado de Pediatria. Madrid: Panamericana, 2015
Pezzella V, et al. Investigation of chronic diarrhoea in infancy. Early Hum Dev 2013; 89: 893-897
Poddighe D. Individual screening strategy for pediatric celiac disease. Eur J Pediatr 2018; 177:187
Ramalho P, Sousa JS. Incidência da doença celíaca em Portugal Continental e Regiões Autónomas (1979-83). Rev Port Pediatr 1990; 21: 147 – 149
Rinawi R, Badarneh B, Tanous O, et al. Elevated anti-tissue transglutaminase antibodies in children newly diagnosed with type 1 diabetes do not always indicate coeliac disease. Acta Paediatrica 2019; 108: 149-153
Watkins RA, Zawahir S. Celiac disease and non celiac gluten sensitivity. Pediatr Clin N Am 2017; 64: 563 – 576
Wong T, White L. Dilemmas in diagnosis and early management of coeliac disease. Paediatr Child Care 2018; 28: 497- 499
Wyllie R, Hyams JS, Kay M (eds). Pediatric Gastrointestinal and Liver Disease. Philadelphia: Elsevier, 2016