Importância do problema
As anomalias congénitas do sistema respiratório, implicando em geral resolução cirúrgica, são situações raras de expressão clínica muito variável.
Com a evolução da tecnologia de imagem aplicada no período pré-natal é hoje possível o diagnóstico antecipado de muitas destas situações, o que contribui para a melhoria do prognóstico.
Etiopatogénese
A morfogénese das estruturas da árvore respiratória (tracto respiratório inferior) que derivam primordialmente do intestino primitivo do embrião, é classicamente dividida em cinco períodos: estes são contados a partir da separação do divertículo “em dedo de luva” ou saccuilus pulmonalis que emerge da face ventral do tubo digestivo primitivo pelos 24 dias de gestação, bifurcando-se pelos 26-28 dias (esboços dos brônquios principais):
- Período embrionário (4ª -7ª semana)
Neste período inicia-se a separação do primórdio respiratório a partir da face ventral do intestino anterior como resultado da formação do septo tráqueoesofágico; estão então constituídos dois “tubos” independentes: o esófago e o tubo laringotraqueal. - Período pseudoglandular (7ª-16ª semana)
Neste período ocorrem determinados eventos em simultâneo: ramificação da árvore respiratória até aos bronquíolos terminais, migração das estruturas vasculares, e desenvolvimento da cartilagem, glândulas mucosas e musculatura lisa nos brônquios a partir do mesênquima. - Período canalicular (16ª-26ª semana)
Neste período formam-se os bronquíolos respiratórios, os ductos alveolares e os alvéolos a partir dos bronquíolos terminais. - Período sacular (26ª-36ª semana)
Os eventos importantes deste período são o crescimento das unidades para as trocas gasosas e a produção de surfactante alveolar. - Período alveolar (a partir da 36ª semana)
Neste período completa- se a formação das estruturas envolvidas na função respiratória continuando o crescimento da superfície de trocas gasosas.
A perturbação deste processo em diversas datas e por efeito de diversos factores dá origem a diversas anomalias congénitas; neste capítulo é feita menção especial a quatro situações deste foro, de possível solução cirúrgica: enfisema lobar congénito, quisto broncogénico, malformação adenomatóide quística e sequestração broncopulmonar.
1. ENFISEMA LOBAR CONGÉNITO
Definição e importância do problema
O enfisema lobar congénito consiste na insuflação anormal de um pulmão anatomicamente normal resultando provavelmente de um defeito intrínseco da cartilagem bronquiolar favorecendo broncomalácia.
Poderá verificar-se compressão extrínseca por anomalias vasculares intratorácicas. Como consequência verifica-se colapso do brônquio afectado durante a expiração levando a retenção progressiva de ar no pulmão por dificuldade de saída daquele. O lobo mais frequentemente afectado é o superior esquerdo (LSE), seguindo-se em frequência o lobo médio direito e o superior direito.
Existem descritos casos raros de compromisso multilobar. Em 50% dos casos não é possível identificar a etiopatogénese. A prevalência do enfisema lobar congénito é ~1/20.000.
Manifestações clínicas
O enfisema lobar congénito pode ser assintomático durante algum tempo (dias), sendo habitual um quadro de dificuldade respiratória, de instalação mais ou menos rápida, nos primeiros dias de vida; é possível que o mesmo seja desencadeado pelo choro. Por vezes a instalação do quadro é aguda.
As manifestações poderão surgir mais tarde, na idade pré-escolar. Podem ocorrer pneumonias recorrentes.
O quadro clínico é explicável pela compressão exercida pelo lobo afectado sobre o pulmão normal.
Exames complementares e diagnóstico diferencial
Esta situação pode ser diagnosticada por ecografia no período pré-natal.
Através da radiografia do tórax realizada perante manifestações de dificuldade respiratória torna-se evidente o sinal de hipertransparência na área do lobo afectado (em geral LSE) com herniação e desvio do mediastino para o lado oposto; a hemicúpula diafragmática homolateral está aplanada (Figura 1).
O diagnóstico diferencial faz-se com pneumotórax e com anomalia adenomatóide quística na sua forma de apresentação de quisto gigante.
A tomografia axial computadorizada ajuda nesta destrinça, bem como esclarece a possível confusão com compressão extrínseca do brônquio por estruturas mediastínicas. Nestes casos a broncoscopia pré-operatória pode tornar-se indispensável.
Poderá estar indicada a cintigrafia de perfusão/ ventilação nos casos de enfisema lobar que se admite tenha sido adquirido após ventilação com pressão positiva de longa duração.
Também está indicada a observação por cardiologista pediátrico que procede a ecografia cardíaca pela elevada probabilidade de associação a anomalia cardiovascular.
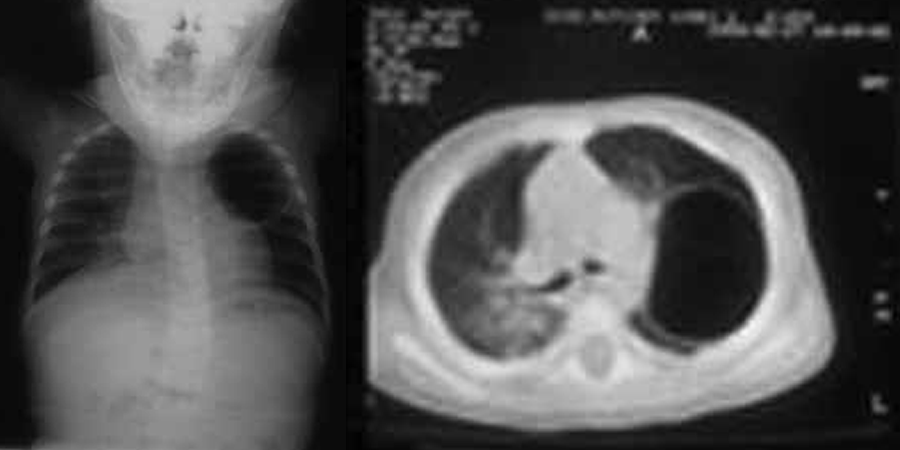
FIGURA 1. Padrão radiográfico convencional do tórax (Enfisema lobar à esquerda). TAC torácica (imagem bolhosa) (NIHDE)
Tratamento
Uma vez comprovado o diagnóstico, o tratamento é cirúrgico.
Se o quadro for de instalação aguda, pode ser necessária uma toracotomia de urgência.
Se se demonstrar que a causa da insuflação é broncomalácia, procede- se a lobectomia. Se existir compressão extrínseca, a intervenção tem como objectivo retirar a causa: com a remoção da causa o lobo afectado retomará a sua função normal.
Se no pré-operatório se tornar indispensável apoio ventilatório, deve ser utilizada ventilação oscilatória de alta frequência.
2. QUISTO BRONCOGÉNICO
Definição
O quisto broncogénico gera-se a partir do divertículo respiratório, em que um grupo de células, que se desenvolve independentemente do tracto respiratório, se separa deste.
Pode ter várias localizações sendo a mais frequente no mediastino posterior ou médio, por de trás ou junto à árvore traqueo-brônquica “mãe” (carina, hilo pulmonar); está frequentemente ligado a esta por um pedículo obliterado ou permeável.
Em geral é central e único.
Pode, raramente, localizar-se no esófago, pericárdio ou no próprio parênquima pulmonar, assumindo nesta última localização a forma multilocular.
No que respeita a características morfológicas, os quistos broncogénicos têm 2 a 10 cm de diâmetro, parede bem individualizada e contêm muco, pus ou sangue.
Manifestações clínicas
Mais frequentemente as manifestações têm início na idade pré-escolar traduzindo- se por sinais de broncospasmo, sinais de compressão, ou por infecções respiratórias de repetição, nalguns casos relacionadas com infecção do próprio quisto quando este comunica com a árvore tráqueo-brônquica.
Os quistos de localização intercarinal podem manifestar-se muito mais precocemente, já no recém-nascido, com insuficiência respiratória, o que implica correcção precoce; podem ser causa de morte súbita.
Noutros casos são assintomáticos, sendo então identificados como achados no âmbito da realização de exame radiográfico do tórax por motivos diversos.
Exames complementares
A radiografia do tórax poderá evidenciar massa paratraqueal ou imagem esferóide com parede fina (semelhante a “balão” ou grande “bolha” correspondente a área de distensão gasosa).
A TAC e a RMN, com maior discriminação imagiológica, possibilitarão a identificação de pequenos quistos intercarinais.
Diagnóstico diferencial
As manifestações clínicas e o padrão radiográfico do tórax convencional evidenciando imagem de distensão gasosa ou “bolhosa” única poderão levar a admitir a presença doutra situação – o quisto pulmonar – com patogénese semelhante ao quisto broncogénico, mas derivando das células do bronquíolo respiratório. O referido quisto pulmonar é, no entanto, periférico (e único) com um padrão radiográfico que evidencia parede melhor definida do que no caso do quisto broncogénico.
Por sua vez, o quisto pulmonar pode confundir-se com pneumatocele o qual apresenta parede menos espessa. O quisto pulmonar, quando infectado, pode confundir-se com abcesso pulmonar.
Tratamento
O tratamento, quer do quisto broncogénico, quer do quisto pulmonar, é a excisão cirúrgica.
3. MALFORMAÇÃO ADENOMATÓIDE QUÍSTICA
Definição e importância do problema
Esta anomalia é caracterizada por crescimento desordenado (histologia de tipo hamartoma ou displasia) dos bronquíolos terminais impedindo quase completamente o crescimento e desenvolvimento alveolar no lobo de um pulmão; como consequência há formação de múltiplos quistos desorganizados alternando com zonas de parênquima não afectado, sendo que os referidos quistos não comunicam com a árvore tráqueo-brônquica e podem comprimir as estruturas vizinhas.
Surge com uma frequência aproximada de 1-4/100.000 nascimentos.
São descritos 3 tipos: 1 (50%), macroquístico, com um ou mais quistos de diâmetro superior a 2 cm; 2 (40%), microquístico com histologia semelhante à do tipo 1; 3 (10%) em que a lesão é sólida simile bronquíolos preenchidos por epitélio cubóide ciliado e não ciliado.
Manifestações clínicas e diagnóstico
As manifestações são precoces, no pós-parto traduzidas por síndroma de dificuldade respiratória conduzindo a insuficiência respiratória; a manifestação mais tardia inaugural pode ser infecção respiratória com recorrências.
A ecografia fetal permite o diagnóstico entre a 12ª e a 14ª semana de vida intra-uterina; por vezes verifica-se inexplicavelmente a sua regressão espontânea o que prova a complexidade de tal anomalia congénita. Em certas formas surge hydrops fetalis.
Após o nascimento a radiografia do tórax é essencial para o diagnóstico definitivo, chamando-se a atenção para o diagnóstico diferencial com a hérnia diafragmática de Bochdaleck (esta última abordada no capítulo 308).
Em casos especiais pode proceder-se à tomografia axial computadorizada.
Tratamento
O tratamento é a excisão cirúrgica – lobectomia – mesmo no doente assintomático, de preferência antes dos 12 meses de idade, face à possibilidade de evolução sarcomatosa ou carcinomatosa.
Quando as lesões são de grandes dimensões pode verificar-se hipoplasia do pulmão e hipertensão pulmonar implicando medidas de suporte respiratório em unidade de cuidados intensivos.
4. SEQUESTRAÇÃO PULMONAR
Definição e etiopatogénese
Esta anomalia é caracterizada pela presença de segmento de parênquima pulmonar não funcionante, sem comunicação evidente com a árvore tráqueo-brônquica; a sua vascularização é anómala, recebendo a totalidade ou a maior parte da sua irrigação arterial sanguínea por vasos oriundos directamente da circulação sistémica.
São descritos dois tipos:
- intralobar em que o tecido sequestrado está contido no lobo normal;
- extralobar, ocorrendo quando a lesão está separada do lobo pulmonar normal e também fora da pleura visceral; este tipo está mais frequentemente associado a outras anomalias congénitas
Manifestações clínicas e diagnóstico
O início das manifestações é muito variável, desde a idade pediátrica à idade adulta. Em geral traduzem-se, quer por sinais e sintomas de infecções respiratórias, quer relacionáveis com shunt de alto débito em relação com os vasos anómalos.
A sintomatologia é predominantemente respiratória, mas a presença de shunts de alto débito, por si só, ou pelas malformações cardíacas congénitas associadas, pode produzir manifestações cardiocirculatórias.
Com efeito, a infecção respiratória é habitual neste tecido pulmonar não funcionante, pelo que as crianças com infecções respiratórias de repetição de causa não evidente devem ser consideradas suspeitas de serem portadoras deste tipo de malformação e investigadas nesse sentido.
A radiografia do tórax convencional, nos casos de tipo intralobar, pode evidenciar sinais de opacidade ou de lesão quística com nível líquido.
A ecografia doppler é o exame de eleição, mas pode haver necessidade de se associar TAC com reconstrução a 3 dimensões, ou ângio-ressonância. (Figura 2)
Deve ser feito o estudo por ecografia e cintigrafia do fígado quando a lesão está localizada na base direita, pois há casos de hérnia diafragmática com fígado intratorácico que podem levar a erros de diagnóstico.
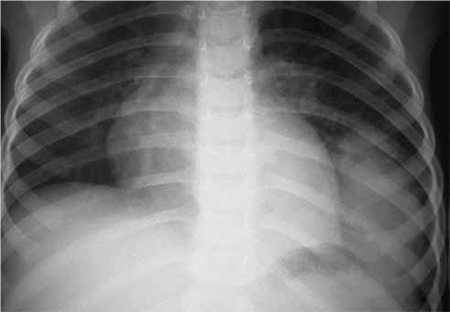
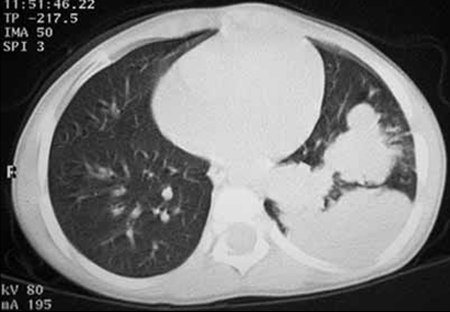
FIGURA 2. Sequestração pulmonar: A – Radiografia do tórax convencional evidenciando opacidade ovóide no terço inferior do hemitórax esquerdo; B – TAC torácica evidenciando opacidades arredondadas confluentes em “mapa geográfico” (NIHDE)
Tratamento
O tratamento da sequestração pulmonar intralobar é a lobectomia ou, caso possível, a segmentectomia, tendo sempre em atenção a necessidade de laquear o vaso anómalo face ao risco de hemorragia e morte intra-operatória.
Os casos de sequestração extralobar que, na sua maioria, são assintomáticos e descobertos por acidente, poderão ser seguidos sem intervenção cirúrgica a qual só estará indicada se se verificar infecção ou sintomatologia cardiocirculatória.
BIBLIOGRAFIA
Calvert JK, Boyd PA, Chamberlain PC, et al. Outcome of antenatally suspected congenital cystic adenomatoid malformation of the lung: 10 years experience 1991-2001. Arch Dis Child 2006; 91: F26-F28
Kliegman RM, Stanton BF, et al (eds). Nelson Textbook of Pediatrics. Philadelphia: Saunders Elsevier, 2015
Goussard P, Green LL, Janson JT, Schubert P. Subcarinal bronchogenic cyst communicating with tracheal bronchial tree, misdiagnosed as pulmonary tuberculosis. Pediatr Pulmonol 2019; 54: 228-229
Landry AM, Rutter MJ. Airway anomalies Clin Perinatol 2018; 45: 597-608
Moro M, Málaga S, Madero L (eds). Cruz Tratado de Pediatria. Madrid: Panamericana, 2015
Rudolph CD, Rudolph AM, Lister GE, First LR, Gershon AA (eds). Rudolph’s Pediatrics. New York: McGraw-Hill Medical, 2011
Sauvat F, Michel JL, Benachi A, et al. Management of asymptomatic neonatal cystic adenomatoid malformations. J Pediatr Surg 2003; 38: 548-552
Schmittenbecher P. Congenital cystic adenomatoid malformation of the lung: Indications and timing of surgery. J Pediatr Surg 2005; 40: 891-892