Definição e importância do problema
A designação estenose aórtica abrange um conjunto de defeitos situados na região da válvula aórtica conduzindo a obstrução, à saída, do fluxo sanguíneo do ventrículo esquerdo; constitui uma forma de lesão obstrutiva esquerda. A estenose aórtica congénita, relacionada com deficiente desenvolvimento embrionário da válvula, tem na sua base etiológica multifactorial. Existe predisposição genética e corresponde a cerca de 5% das anomalias cardíacas. Até há cerca de três décadas a febre reumática era uma causa que explicava as formas adquiridas.
São conhecidos três grandes grupos de lesões com a referida localização: valvular, subvalvular e supravalvular. Pode também ocorrer em associação obstruções a diversos níveis, como na síndroma de Shone, em que se verifica geralmente obstáculo de entrada da válvula mitral, obstáculo subvalvular/valvular aórtico e coarctação da aorta.
1. ESTENOSE AÓRTICA VALVULAR
Epidemiologia e anatomia
Esta situação, na maioria congénita, abrange cerca de 75% dos casos de estenose aórtica e predomina no sexo masculino (relação 4:1). A válvula aórtica pode apresentar-se com uma, duas ou três (raramente quatro) cúspides. Cerca de três quartos dos doentes com estenose valvular possuem válvula bicúspide; esta pode ser funcionalmente normal ou apresentar estenose e regurgitação de grau variável. Com predisposição genética, decorre com doença da parede da aorta (aortopatia) caracterizada por disrupção das fibras elásticas e necrose quística da média.
A válvula aórtica bicúspide corresponde a uma situação evolutiva, evidenciando maior propensão para dilatação da raiz da aorta e da aorta ascendente, e ainda, para dissecção da aorta.
Em cerca de 15% dos doentes existe associação com outras anomalias cardíacas (canal arterial persistente, coarctação da aorta, comunicação interventricular).
Fisiopatologia
A principal consequência fisiopatológica da estenose aórtica é o aumento da pressão do ventrículo esquerdo de forma a manter-se o volume de ejecção, vencendo a sobrecarga de pressão causada pelo obstáculo. Como resposta à sobrecarga de pressão ocorre hipertrofia ventricular esquerda, com compromisso sistólico da função (e geralmente também diastólico) devido a compromisso da distensibilidade do ventrículo esquerdo, o que leva a aumento da pressão telediastólica. Pode, assim, ocorrer dificuldade da perfusão miocárdica, traduzida por isquémia comprometendo ainda mais a função ventricular, em particular em situações de esforço. Quando a hipertrofia e o aumento de pressão já não são suficientes para manter o débito cardíaco, ocorre insuficiência ventricular e surge dilatação ventricular esquerda.
Manifestações clínicas
As manifestações clínicas dependem da repercussão da lesão na redução débito sistémico, causando insuficiência cardíaca e, em casos extremos, síncope.
A forma de apresentação depende da gravidade da estenose e da idade em que se manifesta. A morte súbita é a manifestação clínica mais grave, com um risco estimado em 3 casos / 1.000 / ano.
A forma grave do recém-nascido não produz habitualmente manifestações clínicas de insuficiência cardíaca nos primeiros dias de vida; contudo, com o encerramento do canal arterial, pode estabelecer-se, como consequência do baixo débito cardíaco, um quadro de insuficiência cardíaca global com baixo débito sistémico e com tendência para agravamento progressivo. A intensidade deste quadro e a sua evolução variam com a estrutura e função do ventrículo esquerdo.
A forma mais grave (estenose valvular crítica) apresenta quadro precoce de baixo débito, dependente do canal arterial; as formas mais graves e de prognóstico mais reservado são aquelas em que o ventrículo esquerdo é de pequenas dimensões resultante de fibroelastose por má perfusão in utero. Nesta última situação existe elevado risco de mortalidade intrauterina.
A forma moderada a grave manifesta-se geralmente após o período neonatal com cansaço, taquipneia e hipersudorese durante a alimentação, associados a deficiente progressão ponderal. Na maioria dos casos a doença é oligossintomática, geralmente apenas suspeitada pela detecção de sopro sistólico numa avaliação clínica ocasional.
A forma ligeira é geralmente assintomática, com exame objectivo considerado normal. A doença poderá, por outro lado, ser detectada pela auscultação de sopro sistólico aórtico de ejecção, durante uma avaliação clínica de rotina. De salientar que a progressão da estenose é variável, registando-se casos em que é progressiva e se pode tornar sintomática grave.
De acordo com o que foi referido antes, os achados do exame objectivo poderão variar com a gravidade da estenose, sendo que aquele poderá ser normal. O pulso pode ser parvus (baixa amplitude) e tardus (subida lenta) e o impulso apical sustido. É frequente existir frémito suprasternal e nas carótidas. Na auscultação, o primeiro ruído é normal e o segundo ruído tem desdobramento estreito com intensidade diminuída do componente aórtico. Ausculta-se muitas vezes terceiro ruído. Frequentemente, existe estalido sistólico de abertura da válvula aórtica audível na ponta e bordo esquerdo do esterno. Ausculta-se sopro sistólico de expulsão na porção média do bordo esquerdo do esterno com irradiação para a porção superior do bordo direito e pescoço cuja intensidade é proporcional à gravidade da estenose, excepto se o débito através da válvula for extremamente reduzido.
Exames complementares
Electrocardiograma
As alterações mais frequentes e mais relacionadas com a gravidade da estenose são a hipertrofia e sobrecarga do ventrículo esquerdo: aumento da amplitude de ondas R e evolução progressiva para a inversão das ondas T, com depressão dos segmentos ST. No período neonatal e nos lactentes com formas graves existe frequentemente hipertrofia ventricular direita.
O electrocardiograma dinâmico de Holter deve fazer parte do seguimento dos doentes, pois as arritmias e as perturbações da condução ocorrem com frequência.
A prova de esforço poderá ser útil na avaliação das crianças com formas de estenose moderada, mas com sintomatologia discrepante. A ocorrência de alterações da repolarização, hipotensão, angor, arritmias graves ou síncope relaciona-se com a gravidade da estenose aórtica, podendo estabelecer a indicação para serem adoptadas atitudes interventivas.
Radiografia do tórax
Nas crianças com insuficiência cardíaca pode verificar-se aumento de dimensões da silhueta cardíaca. A cardiomegalia é, no entanto, um marcador pouco sensível da gravidade da estenose. Por vezes observa-se proeminência da aorta ascendente por dilatação pós-estenótica. É rara a calcificação da válvula nas idades pediátricas.
Ecocardiografia
Este exame complementar é actualmente o principal método de diagnóstico de estenose aórtica: permite avaliar a morfologia da válvula, determinar a localização da obstrução e quantificar a sua gravidade. O método Döppler contínuo permite calcular o gradiente de pressões na zona estenosada (inferior a 25 mmHg – estenose não significativa; entre 25 mmHg e 50 mmHg – estenose ligeira; entre 50 mmHg e 75 mmHg – estenose moderada; e superior a 75 mmHg – estenose grave).
É possível determinar a área da válvula aórtica que, por ser independente do débito cardíaco, representa de modo mais fidedigno a gravidade do obstáculo. Uma área efectiva inferior a 0,5 cm2/m2 de superfície corporal traduz estenose grave. (Figura 1)
A ecocardiografia permite ainda avaliar a existência de regurgitação aórtica e detectar a presença de outras anomalias cardíacas.
Em doentes com “má janela” acústica, ou se houver dúvidas sobre aspectos morfológicos da válvula ou da câmara de saída do ventrículo esquerdo, deve utilizar-se a ecocardiografia transesofágica. Para a quantificação da função ventricular e da fracção de regurgitação, quando presente, o melhor método é a angiorressonância magnética.
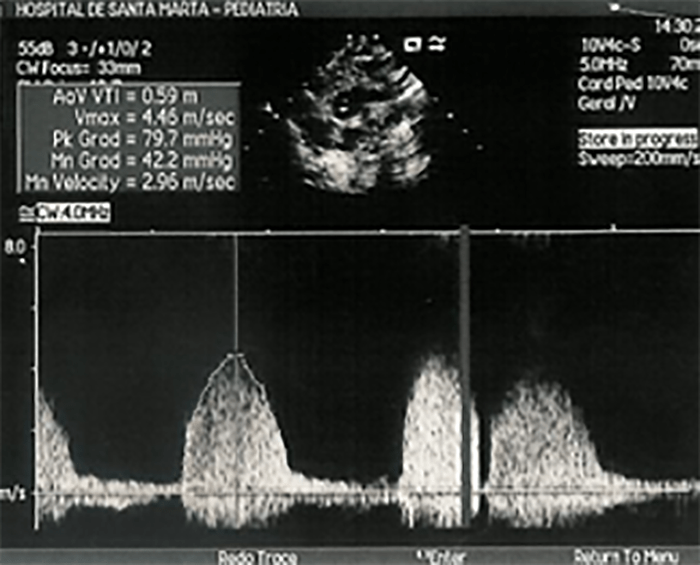
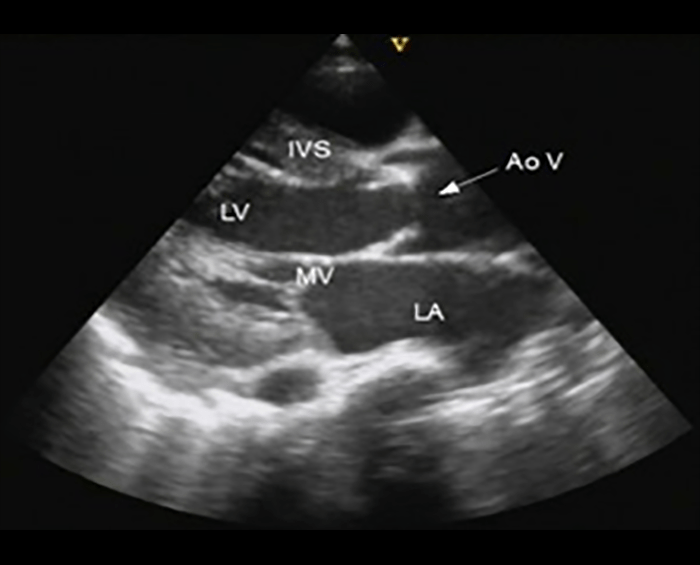
FIGURA 1. Ecocardiografia com avaliação por Döppler contínuo do gradiente através da válvula aórtica (gradiente de pico 79,7 mmHg e médio 42,2 mmHg), à esquerda e plano paraesternal longo mostrando a válvula aórtica espessada (Ao V) e a hipertrofia do septo (ISV) e do ventrículo esquerdo (LV) (MV – válvula mitral e LA – aurícula esquerda)
Tratamento
A actuação nos casos de estenose aórtica (designadamente nas formas de estenose grave e sintomática, ou com alterações electrocardiográficas evidenciando sinais de sobrecarga de pressão ventricular) tem por objectivo a prevenção da disfunção irreversível do ventrículo esquerdo e da morte súbita, assim como o alívio dos sintomas.
O tratamento consiste na eliminação ou diminuição mecânica do obstáculo por: – intervenção cirúrgica, método preferencial em recém-nascidos e lactentes, ou por: – valvuloplastia percutânea de balão, geralmente utilizada em crianças mais velhas e com estenose valvular isolada.
A valvuloplastia percutânea é realizada através da insuflação de um balão na válvula aórtica; a mesma comporta mortalidade média de cerca de 2,4%, mais elevada nos lactentes com menos de 3 meses. Este procedimento é eficaz, com redução de imediato do gradiente transvalvular, mas a longo prazo é grande a taxa de recorrência. A complicação mais frequente é o aparecimento ou o agravamento de insuficiência aórtica.
A vantagem principal da valvuloplastia por balão é adiar a cirurgia, que continuará a ser necessária em muitos doentes.
A cirurgia comporta mortalidade baixa (cerca de 2%), excepto nas formas neonatais graves. Na valvulotomia aumenta-se o orifício aórtico através da separação das comissuras; a mesma associa-se a risco de agravamento da insuficiência aórtica e a reestenose a longo prazo.
A obstrução moderada (gradiente entre 50 e 75 mm Hg) constitui uma “zona cinzenta” que poderá implicar tomar uma atitude interventiva.
Nas crianças em que ainda não haja indicação para intervenção é fundamental manter um seguimento rigoroso, tendo em conta o carácter progressivo da estenose. A actividade física deve ser restringida a esforços ligeiros nas estenoses graves.
Notas importantes:
- Todos os doentes e os portadores de válvula aórtica bicúspide devem ser submetidos a profilaxia da endocardite infecciosa, independentemente da gravidade da estenose, mesmo depois de tratados.
- Gradiente: define-se como diferença de pressões sistólicas entre duas cavidades ou entre duas porções dentro da mesma cavidade, ou vaso sanguíneo. No caso em análise (estenose aórtica), trata-se da diferença de pressões entre o ventrículo esquerdo (VE) e aorta (Ao). Quanto mais grave for a estenose, maior será o gradiente, ou seja, a diferença de pressões entre o VE e Ao.
2. ESTENOSE AÓRTICA SUBVALVULAR
Importância do problema e manifestações clínicas
Os obstáculos subaórticos podem ser provocados por grande variedade de lesões, constituindo os mesmos cerca de 20% das estenoses aórticas; associam-se muitas vezes a comunicação interventricular. O diafragma subaórtico (erradamente designado por “membrana” subaórtica) é o defeito que ocorre com maior frequência. Os doentes estão geralmente assintomáticos e o exame objectivo é semelhante ao da estenose valvular, não havendo, no entanto, estalido sistólico nem alterações do segundo ruído. O sopro sistólico é mais intenso no bordo esquerdo do esterno e, nalguns casos, pode auscultar-se sopro diastólico de insuficiência aórtica.
Exames complementares
A radiografia do tórax habitualmente não apresenta alterações. O electrocardiograma pode ser normal ou apresentar sinais de hipertrofia ventricular esquerda. A ecocardiografia é o melhor método de avaliação, sendo o gradiente de pressões, através do obstáculo, o melhor índice da gravidade da obstrução. (Figura 2)
Tratamento
A actuação é semelhante à descrita para a estenose valvular. Dado que a turbulência provocada pelo obstáculo subaórtico tem efeito lesivo progressivo sobre a válvula aórtica (lesões de “jacto”), a cirurgia está indicada mesmo em casos de estenose moderada desde que haja insuficiência aórtica. A técnica cirúrgica aplicada (ressecção completa do diafragma e miotomia de Morrow) parece diminuir a taxa de recorrência das lesões. Dado que apenas a cirurgia permite remover o diafragma de modo a evitar as lesões de “jacto”, o cateterismo terapêutico não tem tido grande aceitação neste tipo de patologia.
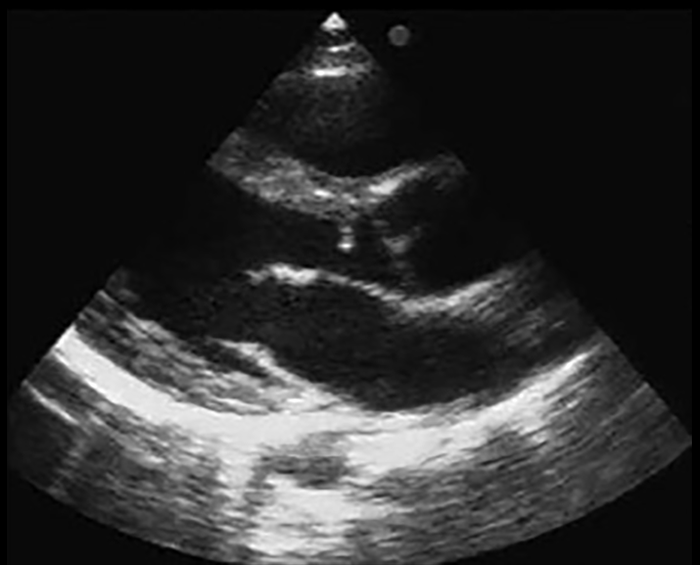
FIGURA 2. Ecocardiograma no plano paraesternal na estenose aórtica subvalvular visualizando-se o diafragma subaórtico
3. ESTENOSE AÓRTICA SUPRAVALVULAR
Importância do problema e manifestações clínicas
Trata-se da forma mais rara de estenose aórtica, representando cerca de 2% dos respectivos casos. Frequentemente associada a perturbações do metabolismo do cálcio, faz parte das alterações que constituem a síndroma de Williams a qual integra, fundamentalmente, fácies característica (de duende), atraso mental, personalidade extrovertida e amigável, hiperacúsia, lábios grossos, e atraso do crescimento. Podendo também ocorrer em crianças sem alterações metabólicas, estão descritas formas familiares. A associação a estenose da origem dos grandes vasos da crossa da aorta, coronárias, artérias subclávias, renais e pulmonares é frequente e deve ser diagnosticada antes da cirurgia. Atribui-se a microdeleções do gene da elastina do cromossoma 7.
Nos doentes sem síndroma de Williams os sintomas são raros. A dispneia e angina ocorrem nas fases avançadas da doença e a síncope é rara. A hipertensão arterial sistémica é comum. Frequentemente encontram-se frémitos nas carótidas, na região supraesternal ou no bordo direito do esterno. Os pulsos periféricos devem ser avaliados com atenção, sendo frequentes pulsações mais intensas na carótida direita e membro superior direito (pelo chamado efeito Coanda provocado pelo jacto de sangue na zona pós-estenótica). Não se ausculta estalido. O sopro sistólico é mais intenso no bordo direito do esterno, irradiando para as carótidas.
Exames complementares
As alterações electrocardiográficas são semelhantes às da estenose valvular. As alterações evidenciadas por radiografia do tórax são também semelhantes, não existindo, no entanto, dilatação pós-estenótica da aorta.
Na ecocardiografia, a visualização do obstáculo é por vezes difícil, sendo no entanto possível detectar a turbulência do fluxo na aorta ascendente e quantificar o gradiente de pressões por eco-Döppler.
A angiorressonância magnética é o método de imagem que melhor permite a identificação da morfologia da lesão, a sua localização, e a identificação de outras estenoses. Raramente poderá ser necessário efectuar cateterismo cardíaco diagnóstico. (Figura 3)
Tratamento
O tratamento é cirúrgico e está indicado se o gradiente for superior a 60 mmHg. A mortalidade é reduzida, estando descritos casos de recorrência da estenose.
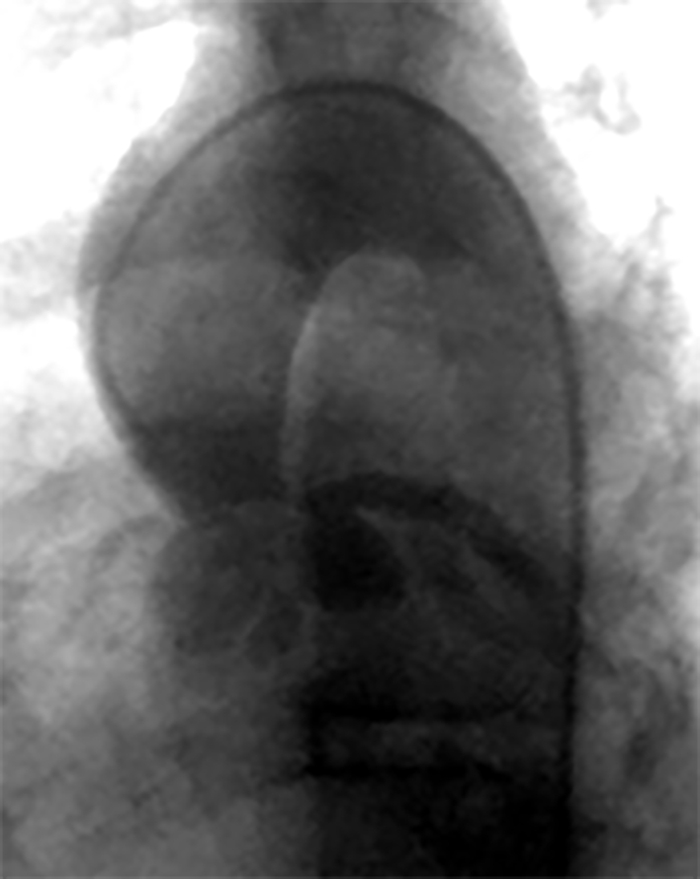
FIGURA 3. Aortografia demonstrando estenose supravalvular aórtica
BIBLIOGRAFIA
Anderson RH, Baker EJ Macartney FJ, Rigby ML, Shinebourne EA, Tynan M (eds). Paediatric Cardiology. London: Churchil Livingstone, 2002
Bonow RO, Carabello B, de León AC, et al. ACC/AHA guidelines for the management of patients with valvular heart disease: a report of the American College of Cardiology/Committee on Management of Patients with Valvular Heart Disease. American Heart Association Task Force on Practice Guidelines. Circulation 1998; 98: 1949-1984
Dia AR, Cifu AS, Shah AP. Management of patients with severe aortic stenosis with transcatheter valve replacement. JAMA 2019; 321: 1527-1528. doi:10.1001/jama.2019.1336
Fiarresga AJ, Kaku S. Estenose aórtica. In Soares-Costa JTS e Kaku S (eds). Cardiopatias Congénitas.Lisboa: Permanyer Portugal, 2005; 67-74
Kliegman RM, StGeme JW, Blum NJ, Shah SS, Tasker RC, Wilson KM (eds). Nelson Textbook of Pediatrics. Philadelphia: Elsevier, 2020
Kline MW, Blaney SM, Giardino AP, Orange JS, Penny DJ, Schutze GE, Shekerdemien LS (eds). Rudolph’s Pediatrics. New York: Mc Graw Hill Education, 2018
Marques C. Diagnóstico das cardiopatias congénitas mais frequentes. In Temas de Pediatria – vol III. Cardiologia Pediátrica. Monografia Beecham. Lisboa: Beecham, 1994; 91-105
Moro M, Málaga S, Madero L (eds). Cruz Tratado de Pediatria. Madrid: Panamericana, 2015
Park MK (ed). Park’s Pediatric Cardiology for practitioners. Philadelphia: Elsevier, 2014
Tweddell JS, Pelech NA, Frommelt PC, et al. Complex aortic valve repair as a durable and effective alternative to valve replacement in children with aortic valve disease. J Thorac Cardiovasc Surg 2005; 129: 551-558